元素之间通过不同的化学键可以组成不同的晶体和化合物。有关化学键与晶体的说法正确的是
| A.两种元素组成的分子中一定只有极性键 |
| B.熔融状态时能导电的化合物一定是离子晶体 |
| C.非金属元素组成的化合物一定是共价化合物 |
| D.分子晶体的熔沸点随着共价键的增强而升高 |
最近发现一种钛原子和碳原子构成的气态团簇分子,如图所示,顶角和面心的原子是钛原子,棱的中心和体心的原子是碳原子,它的化学式为 ( )
| A.Ti14C13 | B.TiC | C.Ti4C4 | D.Ti4C3 |
KO2的晶体结构与NaCl相似,KO2可以看作是Na+的位置用K+代替,Cl-的位置用O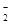 代替,则下列对于KO2晶体结构的描述正确的是
代替,则下列对于KO2晶体结构的描述正确的是
A.与K+距离相等且最近的O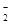 共有8个 共有8个 |
B.与K+距离相等且最近的O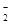 构成的多面体是正八面体 构成的多面体是正八面体 |
| C.与K+距离相等且最近的K+有8个 |
D.一个KO2晶胞中的K+和O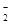 粒子数均为8个 粒子数均为8个 |
下列各组物质的熔沸点按由低到高的顺序排列正确的是
| A.冰、干冰、氯化钠、金刚石 | B.汞、钠、烧碱、二氧化硅 |
| C.NaCl、KCl、CsCl | D.H2O、H2S、H2Se、H2Te |
在下列有关晶体的叙述中正确的是
| A.晶体中有阳离子就一定存在阴离子 |
| B.分子晶体中一定存在共价键和分子间作用力 |
| C.金属晶体的熔点一定比分子晶体高 |
| D.原子晶体中,一定只存在共价键 |
下列说法中错误的是
| A.当中心原子的配位数为6时,配合单元常呈八面体空间结构 |
| B.SO3为平面正三角形结构 |
| C.已知[Cu(NH3)2]2+的中心原子采用sp杂化,则它们的空间构型为直线型 |
| D.配位数为4的配合物均为正四面体结构 |
下列各组物质状态发生变化时,所克服的微粒间作用力完全相同的是
| A.碘的升华和干冰气化 | B.二氧化硅和干冰熔化 |
| C.苯和硝酸钾熔化 | D.食盐的熔化和冰的融化 |
下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是
| A.SO2和Si | B.CO2和H2O |
| C.NaCl和HCl | D.CCl4和KCl |
下列数据是对应物质的熔点: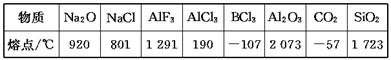
据此做出的下列判断中错误的是( )
| A.铝的化合物的晶体中有的是离子晶体 |
| B.表中只有BCl3和干冰是分子晶体 |
| C.同族元素的氧化物可形成不同类型的晶体 |
| D.不同族元素的氧化物可形成相同类型的晶体 |
下列有关晶体的叙述中,正确的是
| A.在CaF2晶体中,Ca2+、F—的配位数均为8 |
| B.C60晶体中,微粒之间通过共价键结合形成晶体,键角为120° |
| C.在CsCl晶体中,每个Cs+周围紧邻6个C1— |
| D.金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子 |