题目内容
在下列有关晶体的叙述中正确的是
| A.晶体中有阳离子就一定存在阴离子 |
| B.分子晶体中一定存在共价键和分子间作用力 |
| C.金属晶体的熔点一定比分子晶体高 |
| D.原子晶体中,一定只存在共价键 |
D
解析试题分析:A.在金属晶体中有阳离子但是没有阴离子存在。错误。B.在分子晶体中一定存在分子间作用力,但是不一定存在共价键。如惰性气体就是单原子分子,没有化学键存在。错误。C.一般情况下金属晶体的熔点比分子晶体高,但是也有例外。如Hg在常温下是液体,而S单质为分子晶体,熔点S>Hg。错误。D.在原子晶体中,原子间以共价键结合形成空间网状结构,断裂较难,因此熔沸点高,硬度大,难溶于一般的溶剂。正确。
考点:考查晶体结构与化学键的知识。

练习册系列答案
相关题目
已知NaCl、CsCl晶体结构中离子配位数分别为6和8,其中属于从NaCl晶体中分割出来的结构示意图是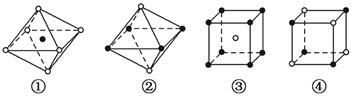
| A.①和③ | B.①和④ | C.只有③ | D.只有④ |
下列有关晶体的叙述中,正确的是
| A.在CaF2晶体中,Ca2+、F—的配位数均为8 |
| B.C60晶体中,微粒之间通过共价键结合形成晶体,键角为120° |
| C.在CsCl晶体中,每个Cs+周围紧邻6个C1— |
| D.金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子 |
水的状态除了气、液和固态外,还有玻璃态。它是由液态水急速冷却到165K(零下108℃)时形成的,玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述正确的是( )
| A.水由液态变为玻璃态,体积缩小 |
| B.玻璃态水变成冰发生化学变化 |
| C.玻璃态是水的一种特殊状态 |
| D.玻璃态水与冰的化学性质不同 |
最近发现,只含镁、镍和碳三种元素的晶体竟然也具有超导性,因这三种元素都是常见元素,从而引起广泛关注。该新型超导晶体的一个晶胞如图所示,则该晶体的化学式为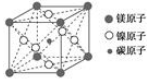
| A.Mg2CNi3 | B.MgCNi3 | C.MgCNi2 | D.MgC2Ni |
下列各组物质的晶体中,化学键种类相同,晶体类型也相同的是
| A.MgO和BaO2 | B.SO2和SiO2 | C.KOH和NH4Cl | D.CCl4和KCl |
下列说法中正确的是(NA为阿伏加德罗常数)( )
| A.28 g晶体硅中含有Si—Si键的个数为2NA |
| B.124 g白磷(P4)晶体中含有P—P键的个数为4NA |
| C.12 g金刚石中含有C—C键的个数为4NA |
| D.SiO2晶体中每1 mol Si可与氧原子形成2NA个共价键(Si—O键) |
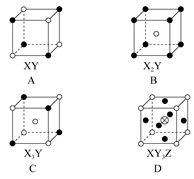
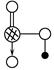 ,请简要说明该物质易溶于水的原因________________________________。
,请简要说明该物质易溶于水的原因________________________________。 —X、
—X、 —Y,
—Y, —Z。其对应的化学式不正确的是( )
—Z。其对应的化学式不正确的是( )