意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的气态N4分子,其分子结构如图所示。已知断裂1mol N—N吸收167kJ热量,生成1mol N≡N放出942kJ热量,根据以上信息和数据,判断下列说法正确的是( )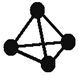
| A.N4属于一种新型的化合物 | B.N4晶体熔点高,硬度大 |
| C.相同质量的N4能量高于N2 | D.1mol N4转变成N2将吸收882 kJ热量 |
下列化合物中,既含有离子键又含有共价键的是
| A.CH3CHO | B.CH3COONH4 | C.SiO2 | D.CaCl2 |
下列分子或离子属等电子体的是
| A.CH4和NH3 | B.NO3-和CO32- | C.H3O+ 和PCl3 | D.CS2和SO2 |
现有如下各说法:( )
①在水分子中氢、氧原子间以共价键相结合;
②活泼金属和活泼非金属化合时一般形成离子键;
③非金属元素间形成的化合物一定是共价化合物;
④根据电离方程式HCl=H++Cl-,判断HCl分子里存在离子键;
⑤冰的密度比水的密度小,这与氢键有关;
上述各种说法正确的是
| A.①②⑤ | B.①②④⑤ | C.①②③④⑤ | D.①③④⑤ |
下列分子中所有原子全部满足最外层为8个电子结构的是( )
| A.PCl5 | B.NH3 | C.PCl3 | D.BF3 |
下列叙述不正确的是( )
| A.原子晶体、离子晶体、金属晶体、分子晶体中都一定存在化学键 |
| B.向煤中加入生石灰可减少对大气的污染 |
| C.完全由非金属元素组成的化合物可以形成离子化合物 |
| D.由氮气为原料合成氨是氮的固定 |
利用相似相溶原理不能解释的是
| A.I2微溶于水,易溶于CCl4;HCl易溶于水 |
| B.在水中的溶解度:C2H5OH>CH3CH2CH2CH2OH |
| C.不同的烃之间相互溶解 |
| D.I2易溶于KI溶液中 |
有关理论认为N2O与CO2分子具有相似的结构(包括电子式);已知N2O分子中氧原子只与一个氮原子相连,下列说法合理的是
| A.N2O与SiO2为等电子体、具有相似的结构(包括电子式) |
B.N2O的电子式可表示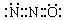 |
| C.N2O与CO2均不含非极性键 |
| D.N2O为三角形分子 |
已知大多数含氧酸可用通式XOm(OH)n来表示,如X是S,则m=2,n=2,则这个式子就表示H2SO4。一般而言,该式中m大于等于2的是强酸,m为0的是弱酸。下列各含氧酸中酸性最强的是
| A.H2SeO3 | B.HMnO4 | C.H3BO3 | D.H3PO4 |
对σ键和π键的认识不正确的是
| A.σ键和π键不属于共价键,是另一种化学键 |
| B.s-sσ键与s-pσ键的电子云均为轴对称图形 |
| C.分子中含有共价键,则至少含有一个σ键 |
| D.含有π键的化合物与只含σ键的化合物的化学性质不同 |