题目内容
下列叙述不正确的是( )
| A.原子晶体、离子晶体、金属晶体、分子晶体中都一定存在化学键 |
| B.向煤中加入生石灰可减少对大气的污染 |
| C.完全由非金属元素组成的化合物可以形成离子化合物 |
| D.由氮气为原料合成氨是氮的固定 |
A
解析试题分析:A项:He等稀有气体为单原子分子,只存在分子间作用力,不存在化学键,错误;B项:生石灰能吸收SO2生成CaSO3,从而减少SO2的排放,正确;C项正确,如NH4Cl等铵盐均为离子化合物;D项正确,氮元素有游离态转化为化合态即为氮的固定。
考点:元素化合物知识与微粒间的作用力。

练习册系列答案
相关题目
下列物质既含离子键又含共价键的是
| A.CO2 | B.NaOH | C.CaCl2 | D.C6H6 |
二氯化二硫(S2C12)可用作橡胶工业的硫化剂,常温下它是橙黄色有恶臭的液体,它的分子结构与H2O2相似,熔点为193 K,沸点为411K,遇水很容易反应,产生的气体能使品红褪色,S2C12可由干燥的氯气通入熔融的硫中制得。下列有关说法不正确的是 ( )
| A.S2C12晶体中不存在离子键 |
| B.S2C12分子中各原子均达到8电子稳定结构 |
| C.S2C12在液态下不能导电 |
| D.S2C12与水反应后生成的气体通入石蕊试液中,现象是溶液先变红后褪色 |
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为
| A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化。 |
| B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道。 |
| C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强。 |
| D.以上说法都不正确。 |
用价层电子对互斥理论预测H2S和CH2O分子的立体结构,两个结论都正确的是
| A.直线形;三角锥形 | B.V形;三角锥形 |
| C.直线形;平面三角形 | D.V形;平面三角形 |
意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的气态N4分子,其分子结构如图所示。已知断裂1mol N—N吸收167kJ热量,生成1mol N≡N放出942kJ热量,根据以上信息和数据,判断下列说法正确的是( )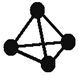
| A.N4属于一种新型的化合物 | B.N4晶体熔点高,硬度大 |
| C.相同质量的N4能量高于N2 | D.1mol N4转变成N2将吸收882 kJ热量 |
下列物质中,既含有离子键又含有极性共价键的是( )
| A.Na2O2 | B.MgCl2 | C.HCl | D.KOH |