关于氢键,下列说法正确的是( )
| A.每一个水分子内含有两个氢键 |
| B.冰、水和水蒸气中都存在氢键 |
| C.分子间形成的氢键使物质的熔点和沸点升高 |
| D.H2O是一种非常稳定的化合物,这是由于氢键所致 |
下列叙述肯定正确的是( )
| A.在离子晶体中不可能存在非极性键 |
| B.在共价化合物的分子晶体中不可能存在离子键 |
| C.在极性分子中不可能存在非极性键 |
| D.在原子晶体中不可能存在极性共价键 |
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为( )
| A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化 |
| B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道 |
| C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强 |
| D.以上说法都不正确 |
下列原子序数所对应的元素组中,两者可形成离子键的是( )。
| A.1和17 | B.12和9 | C.14和6 | D.15和8 |
XY2是离子化合物,X和Y离子电子层结构都与氖原子相同,则X、Y分别为( )。
| A.Ca和Cl | B.K和S | C.Ca和F | D.Mg和F |
以下叙述中错误的是( )。
| A.钠原子和氯原子作用生成NaCl后,其结构的稳定性增强 |
| B.在氯化钠中,氯离子和钠离子靠静电作用结合 |
| C.任何离子键在形成的过程中必定有电子的得与失 |
| D.金属钠与氯气反应生成氯化钠后,体系能量降低 |
(双选)下列说法中正确的是( )。
| A.难失电子的原子,获得电子的能力一定强 |
| B.易得电子的原子所形成的简单阴离子,其还原性一定强 |
| C.活泼金属与活泼非金属化合,易形成离子键 |
| D.电子层结构相同的不同离子,核电荷数越多,半径越小 |
常温下硫单质主要以S8形式存在,加热时S8会转化为S6、S4、S2等,当蒸气温度达到750°C时主要以S2形式存在,下列说法正确的是( )
| A.S8转化为S6、S4、S2属于物理变化 |
| B.不论哪种硫分子,完全燃烧时都生成SO2 |
| C.常温条件下单质硫为原子晶体 |
| D.把硫单质在空气中加热到750°C即得S2 |
SF6是一种无色气体,具有很强的稳定性,可用于灭火。SF6的分子结构如下图所示,呈正八面体型。如果F元素有两种稳定的同位素,则SF6的不同分子种数为 ( )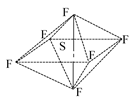
| A.6种 | B.7种 | C.10种 | D.12种 |
三氯化氮(NCl3)是一种淡黄色的油状液体,测得其分子具有三角锥形结构。下列对NCl3的有关描述正确的是( )
| A.NCl3是三角锥形结构,故它是非极性分子 |
| B.NCl3分子间可形成氢键,故它比PCl3难挥发 |
| C.NCl3有孤电子对,它还能以配位键的形式再与一个Cl-结合 |
| D.NCl3分子中不存在非极性共价键 |