题目内容
下列原子序数所对应的元素组中,两者可形成离子键的是( )。
| A.1和17 | B.12和9 | C.14和6 | D.15和8 |
B
解析

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
观察下列模型并结合有关信息,判断有关说法正确的是
| | 硼晶体的结构单元 | SF6分子 | S8分子 | NaCl |
| 结构模型示意图 | 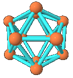 | 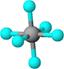 | 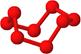 | 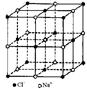 |
| 备注 | 熔点1873K | / | 易溶于CS2 | / |
A.单质硼属分子晶体,其结构单元B12中含有30个B-B键,含20个正三角形
B.SF6是由极性键构成的分子
C.固态硫S8属于原子晶体
D.NaCl熔化和溶于水均能产生自由移动的离子,且破坏的是同种作用力,NaCl晶胞中每个Na+周围最近且等距离的Na+有6个
下列物质只含有离子键的是
| A.CO2 | B.NaOH | C.MgCl2 | D.H2O |
碘具有升华的性质,利用该性质可用于指纹鉴定,因为
| A.汗液中有AgNO3,可以与碘生成黄色沉淀 |
| B.汗液中有NaCl,可以与碘发生化学反应,有颜色变化 |
| C.根据相似相溶原理,碘易溶于皮肤分泌出的油脂中,有颜色变化 |
| D.根据相似相溶原理,碘与汗液中的淀粉有颜色变化 |
下列各分子中,所有原子都满足最外层8电子稳定结构的是( )。
| A.H2O | B.BF3 | C.CCl4 | D.PCl5 |
SF6是一种无色气体,具有很强的稳定性,可用于灭火。SF6的分子结构如下图所示,呈正八面体型。如果F元素有两种稳定的同位素,则SF6的不同分子种数为 ( )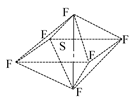
| A.6种 | B.7种 | C.10种 | D.12种 |
观察下表模型并结合有关信息,判断下列说法中不正确的是( )
| | B12结构单元 | SF6分子 | S8分子 | HCN |
| 结构模型示意图 | 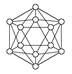 | 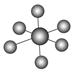 | 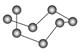 |  |
| 备注 | 熔点1873 K | — | 易溶于CS2 | — |
A.单质硼属于原子晶体,每个B12结构单元中含有30个B—B键和20个正三角形
B.SF6是由极性键构成的非极性分子
C.固态硫S8属于原子晶体
D.HCN的结构式为H—C≡N
将等物质的量的硫酸和氢氧化钠反应后所得到的溶液蒸干,可得到NaHSO4。下列关于NaHSO4的说法中正确的是( )
| A.因为NaHSO4是离子化合物,因此能够导电 |
| B.NaHSO4固体中阳离子和阴离子的个数比是2:1 |
| C.NaHSO4固体熔化时破坏的是离子键和共价键 |
| D.NaHSO4固体溶于水时既破坏离子键又破坏共价键 |
下列叙述错误的是( )。
| A.离子键没有方向性和饱和性,而共价键有方向性和饱和性 |
| B.两种不同的非金属元素可以组成离子化合物 |
| C.配位键在形成时,是由成键双方各提供一个电子形成共用电子对 |
| D.金属键的实质是金属中的“自由电子”与金属阳离子形成的一种强烈的相互作用 |