下列物质的立体结构与NH3相同的是( )
| A.H3O+ | B.H2O | C.CH4 | D.CO2 |
下列化合物中含有手性碳原子的是
| A.CCl2F2 | B.CH3CH3 | C.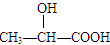 | D.CH3CH2OH |
下列物质中,难溶于CCl4的是 ( )
| A.碘单质 | B.甲烷 | C.苯 | D.水 |
观察下列模型并结合有关信息,判断有关说法正确的是
| | 硼晶体的结构单元 | SF6分子 | S8分子 | NaCl |
| 结构模型示意图 | 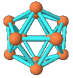 |  |  | 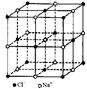 |
| 备注 | 熔点1873K | / | 易溶于CS2 | / |
A.单质硼属分子晶体,其结构单元B12中含有30个B-B键,含20个正三角形
B.SF6是由极性键构成的分子
C.固态硫S8属于原子晶体
D.NaCl熔化和溶于水均能产生自由移动的离子,且破坏的是同种作用力,NaCl晶胞中每个Na+周围最近且等距离的Na+有6个
下列现象与氢键有关的是:
①水结成冰体积膨胀,密度变小
②水加热到很高温度都难以分解
③HF、HCl、HBr、HI的热稳定性依次减弱
④对羟基苯甲醛的沸点高于邻羟基苯甲醛
⑤Cl2、Br2、I2单质熔点随相对分子质量增大而升高
⑥NH3极易溶于水中
| A.①④⑥ | B.①②③④⑤ | C.①④ | D.①②③ |
下列关于化学键的说法中不正确的是
| A.化学键是一种作用力 |
| B.化学键可以使离子相结合,也可以使原子相结合 |
| C.分子间作用力又称范德华力,它属于化学键 |
| D.化学反应过程中,反应物分子内的化学键断裂,生成物分子中的化学键形成 |
下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是
| A.SO2和SiO2 | B.CO2和H2 | C.NaCl和HCl | D.CCl4和KCl |
下列物质只含离子键的是
| A.H2O | B.Na2O | C.NaOH | D.HCl |
下列各组物质,化学键类型相同、晶体类型相同且熔化时破坏作用力类型也相同的 ( )
| A.HCl KCl | B.CO2 SiO2 | C.NH4Cl CCl4 | D.NaOH Na2O2 |
下列说法中不正确的是
| A.含有离子键的化合物一定是离子化合物 |
| B.活泼的金属和活泼的非金属原子之间形成的化学键一定是离子键 |
| C.共价化合物中不可能存在离子键 |
| D.某元素原子最外层只有1个电子,它跟卤素可能形成离子键也可能形成共价键 |