题目内容
下列化合物中含有手性碳原子的是
| A.CCl2F2 | B.CH3CH3 | C.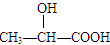 | D.CH3CH2OH |
C
解析试题分析:手性碳原子是连有四个不同的原子或原子团的原子。A.CCl2F2C连有2个Cl原子核2个F原子。因此不含手性碳原子。错误。 B.CH3CH3中的2个C原子都是连接1个C原子核3个H原子,所以不含手性碳原子。错误。C.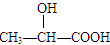 的中间的C原子连接一个甲基、一个羧基、一个羟基、一个H原子,符合手性碳原子的概念。正确。D.CH3CH2OH两个C原子都连接有相同的原子,所以分子中不含手性碳原子。错误。
的中间的C原子连接一个甲基、一个羧基、一个羟基、一个H原子,符合手性碳原子的概念。正确。D.CH3CH2OH两个C原子都连接有相同的原子,所以分子中不含手性碳原子。错误。
考点:考查手性碳原子的概念及判断应用的知识。

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
下列物质中都是既含有离子键又含有共价键的一组是( )
| A.NaOH, H2O, NH4Cl |
| B.KOH, Na2O2, (NH4)2S |
| C.MgO,CaBr2, NaCl |
| D.Na2SO4, HCl, MgCl2 |
下列叙述正确的是( )
| A.离子化合物中一定含有金属元素 |
| B.金属元素不可能存在于阴离子中 |
| C.含有非极性键的化合物不一定是共价化合物 |
| D.由两种元素构成的共价化合物分子中的化学键都是极性键 |
下列对一些实验事实的理论解释正确的是
| 选项 | 实验事实 | 理论解释 |
| A | 氮原子的第一电离能大于氧原子 | 氮原子2p能级半充满 |
| B | CO2为直线形分子 | CO2分子中C—O是极性键 |
| C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是原子晶体 |
| D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是
| A.SO2和SiO2 | B.CO2和H2 | C.NaCl和HCl | D.CCl4和KCl |
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为 ( )
| A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化。 |
| B.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强。 |
| C.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道。 |
| D.氨气分子是极性分子而甲烷是非极性分子。 |
美国科学家合成了含有N5+的盐类,含有该离子的盐是高能爆炸物质,该离子的结构呈“V”形,如图所示。以下有关该物质的说法中正确的是( )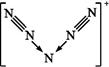
| A.每个N5+中含有35个质子和36个电子 |
| B.该离子中有非极性键和配位键 |
| C.该离子中含有2个π键 |
| D.与PCl4+互为等电子体 |
据新浪科技网报道:美国科学家发现,普通盐水在无线电波的照射下可以燃烧,这很可
能是21世纪人类最伟大的发现之一,将有望解决未来人类的能源危机。无线电频率可以降低盐水中所含元素之间的结合力,释放出氢原子,一旦点火,氢原子就会在这种频率下持续燃烧。上述“结合力”的实质是( )
| A.离子键 | B.共价键 | C.一种静电引力 | D.一种静电斥力 |
下列叙述肯定正确的是( )
| A.在离子晶体中不可能存在非极性键 |
| B.在共价化合物的分子晶体中不可能存在离子键 |
| C.在极性分子中不可能存在非极性键 |
| D.在原子晶体中不可能存在极性共价键 |