下列关于化学键的叙述,正确的一项是( )
| A.离子化合物中一定含有离子键 |
| B.单质分子中均不存在化学键 |
| C.含有极性键的分子一定是极性分子 |
| D.含有共价键的化合物一定是共价化合 |
下列说法正确的是( )
| A.1个甘氨酸分子中存在9对共用电子 |
| B.PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构 |
C.H2(g)+Br2(g)=2HBr(g)△H=-72 kJ·mol-1其它相关数据如下表: 则表中a为230 |
| D.已知S(g)+O2(g)=SO2(s);△H1,S(g)+O2(g)=SO2(g);△H2,则△H2<△H1 |
下列有关化学键的叙述,正确的是( )
| A.分子晶体中一定含有共价键 | B.离子晶体中一定含有离子键 |
| C.含有极性键的分子一定是极性分子 | D.含有共价键的化合物一定是共价化合物 |
CO2的的资源化利用是解决温室效应的重要途径。以下是在一定条件下用NH3捕获CO2生成重要化工产品三聚氰胺的反应:NH3+CO2→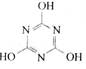 +H2O
+H2O
下列有关三聚氰胺的说法正确的是
| A.分子式为C3H6N3O3 | B.分子中既含极性键,又含非极性键 |
| C.属于共价化合物 | D.生成该物质的上述反应为中和反应 |
X、Y代表两组概念,其关系如下图,下列选项不满足相应关系的是 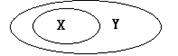
| 选项 | X | Y |
| A. | 氢键 | 化学键 |
| B. | SO2 | 漂白性物质 |
| C. | 油脂 | 酯 |
| D. | 置换反应 | 氧化还原反应 |
下列说法不正确的是
| A.乙烯、苯、溴苯分子中的所有原子均共平面 |
| B.水加热至1000℃以上才分解是因为水分子间存在着氢键 |
| C.常温下浓硫酸和浓硝酸能使铝发生钝化,所以可以用铝槽罐车运输浓硫酸、浓硝酸 |
| D.能发生银镜反应的有机物结构中一定含有-CHO |
下列物质中,所含的原子或离子中最外层都为8电子结构的是
| A.NO2 | B.K2S | C.LiCl | D.CHCl3 |
表中原子化热、晶格能、键能的单位都是kJ·mol-1
| 金属 | 金属原子化热 | 离子化合物 | 晶格能 | 共价键 | 键能 |
| Na | 108.4 | NaCl | 786 | Cl-Cl | 243 |
| Mg | 146.4 | NaBr | 747 | Si-Si | 176 |
| Al | 326.4 | MgO | 3791 | Si-Cl | 360 |
A.Na(s)与Cl2(g)反应生成1molNaCl(s)放出的热量为556.1kJ
B.Si(s)+2Cl2(g)=SiCl4(g) △H= - 602kJ·mol-1
C.从表中可以看出,氯化钠的熔点比晶体硅高
D.从表中数据可以看出,微粒半径越大金属键、离子键的越弱,而共价键却越强
下列说法错误的是
| A.对羟基苯甲酸的沸点比邻羟基苯甲酸高,冰中既存在范德华力,又存在氢键 |
| B.简单立方是非密置层三维堆积形成的,面心立方是由密置层三维堆积形成的 |
| C.所有共价键都有方向性,形成氢键的三个相关原子可以不在直线上 |
| D.金属晶体的导电、导热性都与自由电子有关,离子晶体在一定条件下可以导电 |
有关CH2=CH-C≡N分子的说法正确的是
A.3个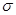 键,3个π键 键,3个π键 | B.4个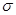 键,3个2π键 键,3个2π键 |
C.6个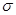 键,2个π键 键,2个π键 | D.6个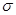 键,3个π键 键,3个π键 |