元素性质呈现周期性变化的基本原因是
| A.元素的原子量逐渐增大 | B.核外电子排布呈周期性变化 |
| C.核电荷数逐渐增大 | D.元素化合价呈周期性变化 |
已知质量数为A的某阳离子Rn+,核外有X个电子,则核内中子数为
| A.A-x | B.A-x-n | C.A-x+n | D.A+x-n |
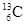 -NMR(核磁共振)可以用于含碳化合物的结构分析。
-NMR(核磁共振)可以用于含碳化合物的结构分析。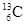 表示的碳原子
表示的碳原子
| A.核外有13个电子,其中4个能参与成键 |
| B.核内有6个质子,核外有7个电子 |
| C.质量数为13,原子序数为6,核内有7个质子 |
| D.质量数为13,原子序数为6,核内有7个中子 |
原子结构模型的演变图中,①为道尔顿实心球式原子模型、②为卢瑟福带核的原子模型、③为汤姆生葡萄干面包式原子模型、④为玻尔轨道式原子模型。其中符合历史演变顺序的一组排列是( )
① ② ③ ④
| A.①③②④ | B.①②③④ |
| C.①④③② | D.①③④② |
下列提出原子学说的科学家是( )
| A.拉瓦锡 | B.道尔顿 | C.门捷列夫 | D.波义耳 |
下列说法中正确的是
| A.第三周期所包含的元素中钠的原子半径最小 |
| B.钠的第一电离能比镁的第一电离能大 |
| C.在所有元素中,氟的电负性最大 |
| D.电子云示意图中的每个小黑点都表示一个电子 |
某种外围电子排布式为2s22p5的元素,下列有关它的描述正确的有
| A.原子序数为7 | B.在周期表中第一电离能最小 |
| C.在周期表中原子半径最小 | D.在周期表中电负性最大 |
X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是
| A.元素Y、Z、W离子具有相同的电子层结构,其半径依次增大 |
| B.元素X与元素Y可以形成两种共价化合物,且这两种化合物只有一种类型的共价键 |
| C.元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR |
| D.元素W、R的最高价氧化物对应水化物都是强酸 |
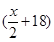 和
和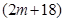
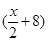 和
和