已知X、Y、Z、W为短周期元素,原子序数依次增大。X、Z同族且均为金属元素,Y、W同族,W的最高价氧化物对应的水化物是强酸。下列说法错误的是
| A.原子半径:Z>W>Y | B.X的最高价氧化物的水化物一定是强碱 |
| C.氢化物的沸点:W—定小于Y | D.Y与Z形成的化合物一定是离子晶体 |
下列说法正确的是
| A.原子的第一电离能越大,该元素的电负性就越大 |
| B.原子的电子层数越多,原子半径越大 |
| C.原子失去电子越多,说明其还原性越强 |
| D.同一原子的能层越高,S电子云的半径越大 |
短周期元素X、Y、Z、W的原子序数依次增大,X和Z同主族,Y和W同主族,原子半径X小于Y,四种元素原子最外层电子数之和为14。下列叙述正确的是
| A.气态氢化物的热稳定性:HnY>HnW |
| B.同周期元素中W的最高价氧化物对应水化物的酸性最强 |
| C.Y和X、Z和X组成的常见化合物中化学键的类型相同 |
| D.原子半径的大小顺序: rW>rZ>rY>rX |
几种短周期元素的原子半径及主要化合价如下表 ( )
| 元素代号 | X | Y | Z | M | N | P |
| 原子半径/nm | 0.186 | 0.143 | 0.075 | 0.074 | 0.152 | 0.099 |
| 元素的主要化合价 | +1 | +3 | +5、-3 | -2 | +1 | +7、-1 |
下列叙述错误的是(其中NA表示阿伏加德罗常数的值)
A.X、N元素的金属性:X>N
B.Y、M元素形成的离子化合物是工业冶炼Y的原料
C.X单质在M单质中燃烧生成的化合物39g中共含有0.5NA个阴离子
D.标准状况下1L 1mol·L-1的YP3溶液中含有NA个Y3+离子
甲、乙、丙、丁、戊为短周期原子序数依次增大的五种主族元素。乙、戊同主族,甲与乙的原子序数之和等于戊的原子序数。丙是短周期主族元素中原子半径最大的元素,丁元素在地壳中含量居金属元素的第一位。下列说法正确的是
| A.简单离子半径:丁>丙>乙>甲 |
| B.气态氢化物的稳定性:甲>乙 |
| C.甲与丙形成的化合物仅有一种 |
| D.丙、丁、戊的最高价氧化物对应的水化物之间两两均能反应 |
有一个未完成的离子方程式: +XO3-+6H+=3X2+3H2O。据此判断下列说法中正确的是
| A.X可能是周期表中第二周期元素 |
| B.X元素的原子最外层上有7个电子 |
| C.X2是还原产物,H2O是氧化产物 |
| D.若生成3 mol X2,转移6 mol电子 |
下列说法正确的是
A.H与D,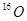 与 与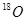 互为同位素: 互为同位素: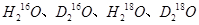 互为同素异形体 互为同素异形体 |
| B.元素X含氧酸的酸性强于元素Y的含氧酸的酸性,则X的得电子能力强于元素Y |
| C.质量数相同的不同核素,一定属于不同种元素 |
D.常温下,在pH=1的溶液中,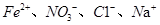 能够大量共存 能够大量共存 |
已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物稳定性大于Z的气态氢化物稳定性,X、Y为金属元素,X单质的还原性大于Y的单质的还原性。下列说法正确的是
| A.W与X形成的化合物中只含离子键 |
| B.W的气态氢化物的沸点一定高于Z的气态氢化物的沸点 |
| C.X、Y、Z、W的原子半径依次减小 |
| D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |
X、Y、Z、R、W是原子序数依次增大的五种短周期元素。Y和R同主族,可组成共价化合物RY2,Y和Z最外层电子数之和与W的最外层电子数相同,25℃时,0.1mol/L X和W形成化合物的水溶液pH为1。下列说法正确的是
| A.由于非金属性Y>R,所以X、Y组成化合物的沸点高于X、R组成的化合物 |
| B.Y和其他四种元素均可形成至少两种的二元化合物 |
| C.RY2能与Y、Z形成的一种化合物反应生成Y2 |
| D.Y、Z、W三种元素组成化合物的水溶液一定显碱性 |
下列说法中,正确的是
| A.I A族元素的金属性比ⅡA族元素的金属性强 |
| B.ⅥA族元素的氢化物中,最稳定的氢化物常温时为无色液体 |
| C.某主族元素X的气态氢化物化学式为HX,则其最高正价为+7价 |
| D.金属元素的原子只有还原性,金属阳离子只有氧化性 |