右图为元素周期表中短周期的一部分,下列说法正确的是 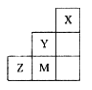
| A.非金属性:Y>Z>M |
| B.离子半径:M->Z2->Y- |
| C.ZM2分子中各原子的最外层均满足8电子稳定结构 |
| D.三种元素中,Y的最高价氧化物对应的水化物酸性最强 |
能说明氯的非金属性比溴强的事实是( )
①共用电子对偏移程度:H-Cl > H-Br ②酸性:HClO4 > HBrO4
③热稳定性:HCl > HBr ④酸性:HCl <HBr
| A.①②③ | B.①②④ | C.②③④ | D.②③ |
短周期元素W、X、Y和Z的原子序数依次增大。金属W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y的单质是常见的金属,可做海洋电池的负极材料。Z原子的质子数是同主族上一周期原子质子数的2倍。下列说法正确的是( )
| A.由金属W制备的高效电池可用NH4Cl溶液作电解质 |
| B.元素X与氢形成的化合物中不可能既有极性健又有非极性健 |
| C.元素Y、Z分别形成的简单离子,后者的离子半径较前者大 |
| D.元素Y、Z的最高价氧化物对应的水化物之间不能反应 |
四种短周期元素在周期表中的位置如右图,其中只有M为金属元素。下列说法不正确的是
| A.原子半径Z<M |
| B.Y的最高价氧化物对应水化物的酸性比X 的弱 |
| C.X 的最简单气态氢化物的热稳定性比Z的小 |
| D.Z位于元索周期表中第2 周期、第ⅥA族 |
X、Y、Z、W四种短周期主族元素的原子序数依次增大,X在短周期中原子半径最大,Y是地壳中含量最高的金属元素,Z的最高正化合价与最低负化合价的代数和为4。下列说法正确的是( )
| A.气态氢化物的稳定性:Z<W |
| B.X与W形成的化合物中含有共价键 |
| C.最高价氧化物对应水化物的碱性:X<Y |
| D.Y的氧化物不能与X的最高价氧化物的水化物发生反应 |
如图是元素周期表短周期元素的一部分。已知M最高价氧化物对应的水化物为常见的氧化性酸,下列说法正确的是: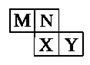
| A.M为氮元素 |
| B.原子半径:Y>X |
| C.氢化物沸点:X>N |
| D.M、X、Y三种元素的最高价氧化物对应的水化物均为强酸 |
据下表信息,判断以下叙述正确的是( ) 部分短周期元素的原子半径及主要化合价
| 元素代号 | G | L | M | Q | R | T |
| 原子半径/nm | 0.186 | 0.160 | 0.143 | 0.104 | 0.075 | 0.066 |
| 主要化合价 | +1 | +2 | +3 | +6、-2 | +5、-3 | -2 |
A.GOH溶液和M(OH)3可以相互反应
B.非金属性:T<Q
C.气态氢化物的稳定性:R>T
D.L2+与T2-核外电子数相等
短周期元素W、X、Y、Z的原子序数依次增大,其简单离子都能破坏水的电离平衡的是
| A.W2-、X+ | B.X+、 Y3+ | C.Y3+、 Z2- | D.X+、 Z2- |
X、Y、Z、W是分别位于第2、3周期的元素,原子序数依次递增。X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14。下列说法正确的是
| A.原子半径由小到大的顺序:X< Y < Z< W |
| B.Z的最高价氧化物能与水反应生成相应的酸 |
| C.Y单质在一定条件下可以与氧化铁发生置换反应 |
| D.室温下,0.1 mol/L W的气态氢化物的水溶液的pH > 1 |