下列有关化学用语表示正确的是( )
| A.乙烯的结构简式为C2H4 |
B.质子数为53,中子数为78的碘原子: |
C.S2-的结构示意图: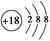 |
D.NH4Cl的电子式为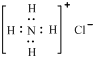 |
X、Y为短周期元素,X原子各电子层的电子数比为1∶4∶1,它比Y原子多3个电子。下列叙述错误的是( )
| A.X离子半径小于Y离子半径 |
| B.X单质在空气中燃烧不止生成一种化合物 |
| C.Y的氢化物的稳定性比同族元素的高 |
| D.X、Y形成的化合物属于共价化合物 |
已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强,下列说法正确的是( )
| A.化合物XZW既含离子键也含共价键 |
| B.对应气态氢化物的稳定性Y>Z |
| C.对应简单离子半径:X>W |
| D.Y的氧化物能与Z或X的最高价氧化物对应的水化物反应 |
在周期表主族元素中,甲元素与乙、丙、丁三元素紧密相邻(上下或左右),甲、乙两元素的原子序数之和等于丙元素的原子序数,这四种元素原子的最外层电子数之和为20。下列说法正确的是( )
| A.甲、乙、丙、丁四种元素均为短周期元素 |
| B.气态氢化物的稳定性:甲>乙 |
| C.最高价氧化物对应的水化物的酸性:甲<丙 |
| D.元素丁与乙形成的化合物中可能含有离子键 |
下列有关元素的性质及其递变规律正确的是( )
| A.ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物 |
| B.第二周期元素从左到右,最高正价从+1递增到+7 |
| C.同主族元素的简单阴离子还原性越强,水解程度越大 |
| D.同周期金属元素的化合价越高,其原子失电子能力越强 |
元素X形成的离子与钙离子的核外电子排布相同,且X的离子半径小于负二价硫离子的半径,X元素为( )
| A.Al | B.P | C.Ar | D.K |
短周期元素X、Y、Z、W、Q在元素周期表的位置如表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法中正确的是( )
| X | | Y | |
| Z | | W | Q |
A.钠与W可能形成Na2W2化合物
B.由Z与Y组成的物质在熔融时能导电
C.W得电子能力比Q强
D.X有多种同素异形体,而Y不存在同素异形体
金属钛对体液无毒且有惰性,能与肌肉和骨骼生长在一起,因而有“生命金属”之称。下列有关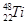 和
和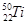 的说法中正确的是( )
的说法中正确的是( )
A.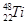 和 和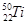 中均含有22个中子 中均含有22个中子 |
B.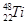 和 和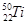 核外均有4个电子层 核外均有4个电子层 |
C.分别由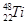 和 和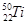 组成的金属钛单质互称为同分异构体 组成的金属钛单质互称为同分异构体 |
D.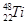 和 和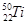 的性质完全相同 的性质完全相同 |
X、Y、Z、W是分别位于第2、3周期的元素,原子序数依次递增。X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14。下列说法正确的是( )
| A.原子半径由小到大的顺序:X<Y<Z<W |
| B.Y单质在一定条件下可以与氧化铁发生置换反应 |
C.室温下,0.1 mol·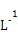 W的气态氢化物的水溶液的pH>1 W的气态氢化物的水溶液的pH>1 |
| D.Z的最高价氧化物能与水反应生成相应的酸 |