某粒子结构示意图为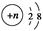 ,若该粒子为离子,则它所带的电荷数可能为( )。
,若该粒子为离子,则它所带的电荷数可能为( )。
①8-n ②n-8 ③10-n ④n-10
| A.①② | B.①③ | C.③④ | D.②④ |
下列叙述错误的是( )。
| A.在所有元素中氢原子半径最小 |
| B.Al3+、Na+、O2-微粒半径依次增大 |
| C.P、S、Cl最高正价依次升高 |
| D.锂、钠、钾、铷、铯单质的熔点逐渐升高 |
几种短周期元素的原子半径和主要化合价见下表,下列说法中正确的是( )。
| 元素代号 | 原子半径/nm | 主要化合价 |
| X | 0.160 | +2 |
| Y | 0.143 | +3 |
| Z | 0.102 | +6、-2 |
| L | 0.099 | +7、-1 |
| M | 0.077 | +4、-4 |
| Q | 0.074 | -2 |
A.等物质的量的X、Y的单质与足量的盐酸反应,生成的H2一样多
B.Y与Q形成的化合物不能跟氢氧化钠溶液反应
C.Z的氢化物的稳定性强于L的氢化物的稳定性
D.在化学反应中,M原子与其他原子易形成共价键而不易形成离子键
下列说法中,正确的是( )。
| A.周期表中的主族都有非金属元素 |
| B.周期表中的主族都有金属元素 |
| C.周期表中的非金属元素都位于主族(除稀有气体) |
| D.周期表中的非金属元素都位于短周期 |
元素周期表是一座开放的“元素大厦”,“元素大厦”尚未客满。若发现119号元素,请在“元素大厦”中安排好它的“房间”( )。
| A.第七周期0族 | B.第六周期第ⅡA族 |
| C.第八周期第ⅠA族 | D.第七周期第ⅦA族 |
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如下图所示。下列说法正确的是( )。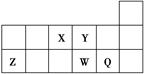
| A.元素X与元素Z的最高正化合价之和的数值等于8 |
| B.原子半径的大小顺序为rX>rY>rZ>rW>rQ |
| C.离子Y2-和Z3+的核外电子数和电子层数都不相同 |
| D.元素W的最高价氧化物对应的水化物酸性比Q的强 |
X、Y、Z是三种短周期元素,其中X、Y位于同一主族,Y、Z处于同一周期。X原子的最外层电子数是其电子层数的3倍。Z原子的核外电子数比Y原子少1。下列说法正确的是( )。
| A.元素非金属性由弱到强的顺序为Z<Y<X |
| B.Y元素最高价氧化物对应水化物的化学式可表示为H3YO4 |
| C.三种元素的气态氢化物中,Z的气态氢化物最稳定 |
| D.原子半径由大到小的顺序为Z<Y<X |
运用元素周期律分析下面的推断,其中错误的是( )。
| A.铍(Be)的氧化物的水化物可能具有两性 |
| B.砹(At)为白色固体,HAt不稳定,AgAt感光性很强 |
| C.硫酸锶(SrSO4)是难溶于水的白色固体 |
| D.硒化氢(H2Se)无色、有毒,比H2S更不稳定 |