X、Y、Z、W四种元素在元素周期表中的相对位置如下图所示,其中X、W的质子数之和为21,由此可知
| | X | | Y |
| Z | | W | |
A.X位于元素周期表中第2周期、第ⅤA族
B.Y的氢化物(H2Y)不稳定,100℃以上即可分解
C.Z的最高价氧化物的水化物是一种强碱
D.W的非金属性比Y的非金属性弱
W、X、Y、Z为原子序数递增的四种短周期元素。W是原子半径最小的元素,X的一种核素在考古时常用来鉴定一些文物的年代,Y是植物生长所需化学肥料中主要的营养元素之一,Z原子的最外层电子数是X原子最外层电子数的1.5倍。下列说法正确的是:
| A.氢化物的沸点:Z一定高于Y |
| B.最高价氧化物对应水化物的酸性:X强于Y |
| C.仅由W、Y、Z三种元素组成的化合物不可能属于盐类 |
| D.W、X、Y、Z都能分别与氯元素形成共价化合物 |
下列说法中正确的是 ( )
| A.第三周期所包含的元素中钠的原子半径最小 |
| B.钠的第一电离能比镁的第一电离能大 |
| C.在所有元素中,氟的电负性最大 |
| D.电子云示意图中的每个小黑点都表示一个电子 |
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是 ( )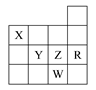
| A.常压下五种元素的单质中W单质的沸点最高 |
| B.Z元素的最高价氧化物对应的水化物酸性最强 |
| C.X的氢化物比同族元素的氢化物沸点低 |
| D.Y、Z和W的阴离子半径依次增大 |
X、Y、Z为短周期元素,原子序数依次增大。X的最外层电子数是Y原子最外层电子数的2倍,质子数比Y少5,X、Z在同主族。下列叙述不正确的是( )
| A.原子半径:Y>Z |
| B.X元素的一种单质可用于消毒杀菌 |
| C.Y的氧化物是工业制取Y单质的主要原料 |
| D.Z的单质在氧气中点燃可生成两种酸性氧化物 |
A元素的阳离子与B元素的阴离子具有相同的电子层结构,关于两元素有以下叙述:①原子半径A<B;②离子半径A>B;③原子序数A>B;④原子最外层电子数A<B;⑤A的正化合价与B的负化合价的绝对值一定相等。其中正确的是 ( )
| A.①② | B.③④ | C.③⑤ | D.③④⑤ |
下列结论不正确的是 ( )
| A.微粒半径:S>S2->Cl->F |
| B.酸性:HClO4>H2SO4>H3PO4 |
| C.氧化性:Cl2>S>Se>Te |
| D.离子还原性:S2->I->Br->OH- |
依据元素周期律及元素周期表知识,下列推断正确的是 ( )
| A.酸性:H2SiO3>H2CO3 |
| B.热稳定性:H2Se>H2S>H2O |
| C.碱性:CsOH>Ca(OH)2 |
| D.若离子半径:R2->M+,则原子序数:R>M |