四种短周期元素W、X、Y、Z的原子序数依次递增,X的一种单质能在空气中自燃。电解含有Y和Z的阴离子的混合溶液时,在阳极Y离子先失去电子。W和Z同主族。对于这四种元素下列判断正确的是
| A.气态氢化物的稳定性:W>X>Y>Z |
| B.单质的氧化性:W>Z>Y>X |
| C.四种元素原子半径大小:W<Y<Z<X |
| D.W单质可以将Z从其盐溶液中置换出来 |
下列说法正确的是
| A.非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价 |
| B.只有非金属能形成含氧酸或含氧酸盐 |
| C.除稀有气体外的非金属元素都能生成不同价态的含氧酸 |
| D.非金属的最高价含氧酸都具有强氧化性 |
下列说法中,不符合ⅦA族元素性质特征的是
| A.从上到下原子半径逐渐减小 | B.易形成-1价离子 |
| C.最高价氧化物的水化物显酸性 | D.从上到下氢化物的稳定性依次减弱 |
X元素最高氧化物对应的水化物为H3XO4,则它对应的气态氢化物为
| A.HX | B.H2X | C.XH4 | D.XH3 |
下列分子中所有原子都满足最外层为8个电子结构的是
| A.BF3 | B.CCl4 | C.H2O | D.PCl5 |
已知R2+离子核外有a个电子,b个中子。表示R原子符号正确的是
A. | B.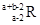 | C.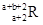 | D.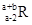 |
根据表中提供的部分短周期元素原子半径及主要化合价的信息,判断以下叙述中正确的是:
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.氢化物的沸点为H2T<H2R
B.单质与稀盐酸反应的速率为L>Q
C.M与T形成的化合物具有两性
D.L2+与R2-的核外电子数相等
下列递变规律正确的是:
| A.HClO4、H2SO4、H3PO4的酸性依次增强 |
| B.P、S、Cl最高正价依次升高 |
| C.HCl、HBr、HI的稳定性依次增强 |
| D.锂、钠、钾的金属性依次增强 |
能说明A元素的非金属性比B元素的非金属性强的是:
| A.A原子得到电子的数目比B原子少 |
| B.A元素的最高正价比B元素的最高正价要高 |
| C.气态氢化物溶于水后的酸性:A比B强 |
| D.A单质能与B的氢化物水溶液反应,生成B单质 |
下列微粒半径大小比较正确的是:
| A.Na+<Mg2+<Al3+<O2- | B.S2->Cl->Na+>Al3+ |
| C.Na<Mg<Al<S | D.Ca<Rb<K<Na |