题目内容
根据表中提供的部分短周期元素原子半径及主要化合价的信息,判断以下叙述中正确的是:
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.氢化物的沸点为H2T<H2R
B.单质与稀盐酸反应的速率为L>Q
C.M与T形成的化合物具有两性
D.L2+与R2-的核外电子数相等
BC
解析试题分析:根据元素的原子半径及元素的化合价可推知:L是Mg;M是Al; Q是Be;R是S;T是O。A.O、S是同一主族的元素,由于非金属性O>S。两元素的氢化物H2O、H2S都是由分子构成的物质。由于O的电负性大,而原子半径小,所以在水分子之间除了存在分子间作用力外,还存在着氢键。而H2S的分子间只存在分子间作用力。因此沸点H2O>H2S。错误。B.金属性Mg>Al.元素的金属性越强,其与酸发生反应时速率就越快。因此与同浓度的盐酸反应速率Mg>Al.正确。C.Al2O3是两性氧化物,既能与强酸反应产生盐和水,也能与强碱反应产生盐和水。正确。D.Mg2+的核外电子排布为2、8;与S2-的核外电子电子排布为2、8、8。因此核外电子数不相等。错误。
考点:考查元素的推断及元素形成的物质会微粒的性质比较的知识。

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,其最外层电子数之和等于24,由此可知说法错误的是( )
| W | X | |
| | Y | Z |
A.原子半径大小:W>X
B.元素最高正价:W>Z
C.简单阴离子的还原性:Y>Z
D.气态氢化物的稳定性:X>Y
镭是元素周期表中第ⅡA族元素,下列关于镭的叙述不正确的是
| A.镭比钙的金属性更强 | B.在化合物中呈+2价 |
| C.镭是一种放射性元素 | D.氢氧化镭呈两性 |
1992年,我国取得重大科技成果之一就是发现了三种元素新的同位素,其中一种是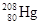 ,它的中子数为:
,它的中子数为:
| A.80 | B.288 | C.208 | D.128 |
下列排序正确的是
| A.酸性:H3AsO4> H2SO4>H3PO4 | B.碱性:Ba(OH)2<Ca(OH)2<KOH |
| C.熔点:MgBr2<SiCl4<SiC | D.沸点:PH3<NH3<H2O |
下列说法正确的是
| A.非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价 |
| B.只有非金属能形成含氧酸或含氧酸盐 |
| C.除稀有气体外的非金属元素都能生成不同价态的含氧酸 |
| D.非金属的最高价含氧酸都具有强氧化性 |
下列说法正确的是
| A.金属元素和非金属元素间形成的化学键一定是离子键 |
| B.ⅦA族元素是同周期元素中非金属性最强的元素 |
| C.全部由非金属元素形成的化合物一定是共价化合物 |
| D.短周期中,同周期元素的离子半径从左到右逐渐减小 |