a、b、c、d、e为元素周期表前3周期中的部分元素,它们在元素周期表中的相对位置如图所示。下列叙述正确的是( )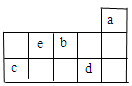
| A.b元素除0价外,只有一种化合价 |
| B.五种元素中,c元素的单质性质最稳定 |
| C.d气态氢化物的水溶液既有氧化性也有还原性 |
| D.e元素最高价氧化物对应的水化物是一种强酸,保存在无色试剂瓶里 |
L—T 5种短周期元素的信息如下表,有关叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、+4、-2 | -2 |
A.与稀盐酸反应的剧烈程度:L单质<Q单质
B.热稳定性:H2T<H2R
C.沸点:H2T>H2R
D.L2+与R2-的核外电子数相等
下列排列顺序不正确的是
| A.熔点:Al>K>Na | B.微粒的半径:Cl- >Na+>Mg2+>Al3+ |
| C.热稳定性:HF>HCl>HBr>HI | D.结合质子能力:AlO-2>CO32->F- |
短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电予数之和为l3。X的原子半径比Y的小,X与W同主族,Z是地壳中含量最高的元素。下列说法正确的是
| A.原子半径的大小顺序:r(Y)>r(Z)>r(W) |
| B.元素Z、W的简单离子的电子层结构不同 |
| C.元素Y的简单气态氢化物的热稳定性比Z的强 |
| D.只含X、Y、Z三种元素的化合物,可能是离子化合物,也可能是共价化合物 |
氡是放射性稀有气体元素,氡气吸入体内有害健康,氡的核电荷数是86,相对原子质量是222。科学家还发现某些放射性矿物分解放出的“锕射气”,是由质子数86,质量数219的原子组成,下列有关氡的说法正确的是
A.氡气在标准状况下密度约是19.82g |
| B.氡气化学性质较活泼,因此对人体有害 |
| C.氡原子核外有7个电子层,最外层有8个电子 |
| D.“锕射气”是氡的同位素 |
X、Y、Z、W为四种短周期元素,它们在周期表中的位置如图所示。Z元素原子核外第一层与第三层电子数相等。下列说法不正确的是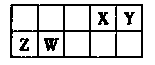
| A.与相同浓度的盐酸反应,Z单质比W单质更剧烈 |
| B.Y元素可以形成多种具有漂白性的化合物 |
| C.Y与Z、Y与W形成的化合物含有的化学键类型相同 |
| D.四种元素的离子半径大小为Z>W>X>Y |
短周期元素R、T、Q、W、G在元素周期表中的相对位置如图所示,其中Q是无机非金属材料的主角。下列判断正确的是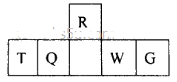
| A.离子半径:T< W<G |
| B.等物质的量的W、G单质分别与足量铁粉反应,后者消耗的铁粉多 |
| C.最简单气态氢化物的热稳定性:Q<R |
| D.T和G组成的化合物溶于水,其水溶液呈中性 |
已知X,Y声是元素周期表中前20号元素:|x-y|="3," X, Y能形成化合物M,下列说法正
确的是
| A.若X和Y处于同一周期,则X的原子半径肯定小于Y的原子半径 |
| B.若X和Y处于不同的周期,则M溶于水所得溶液肯定呈碱性 |
| C.若M属于共价化合物,则该分子中原子个数比可能为1:2 |
| D.若M属于离子化合物,则该化合物中只存在离子键 |
X、Y、Z、Q、W均为短周期元素,原子序数逐渐增大。X、Q同主族,Q元素的焰色反应为黄 色;W的原子半径是同周期中最小的;X与Y、Z分别形成化合物甲、乙,甲、乙均由10电子分子构成,且能反应生成碱。下列说法不正确的是
| A.X的单质和Q的单质均可用电解法制得 |
| B.X与Z可形成同时含有极性键和非极性键的化合物 |
| C.Q与W形成的化合物熔化或溶于水时均可发生电离 |
| D.X、Y、Z三种元素形成的化合物一定能抑制水的电离 |