下列说法正确的是
| A.短周期元素形成离子后,最外层均达8电子稳定结构 |
| B.多电子原子中,在离核较近的区域运动的电子能量较低 |
| C.非金属元素组成的化合物中只有共价键 |
| D.HF、HCl、HBr、HI的热稳定性和还原性依次增强 |
短周期元素X、Y、Z三种原子核外电子总数为32,都可形成常温下气体单质。X原子最外层电子数是其内层电子数的3倍;Y的气态氢化物与其最高价氧化物对应的水化物恰好反应的产物只有一种A,A的水溶液显酸性。下列说法正确的是
| A.原子半径: Z>X >Y |
| B.X元素形成的单质其摩尔质量一定是32g·moL-1 |
| C.物质A中既含离子键又含共价键 |
| D.YX2、ZX2都有对应的含氧酸 |
下表列出了某短周期元素R的各级电离能数据(用I1、I2表示,单位为kJ·mol-1)。
| | I1 | I2 | I3 | I4 | …… |
| R | 740 | 1 500 | 7 700 | 10 500 | …… |
A、R的最高正价为+3价 B、R元素位于元素周期表中第ⅡA族
C、R元素的原子最外层共有4个电子 D、R元素基态原子的电子排布式为1s22s2
下列物质的沸点逐渐升高的是
| A.NH3 PH3 AsH3 SbH3 | B.Si SiC H2O CO2 |
| C.NaI NaBr NaCl NaF | D.Li Na K Rb |
下列说法中错误的是
| A.SO2、SO3都是极性分子 |
| B.在NH4+和[Cu(NH3)4]2+中都存在配位键 |
| C.元素电负性越大的原子,吸引电子的能力越强 |
| D.PCl3和NF3分子中所有原子的最外层都达到8电子稳定结构 |
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是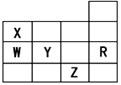
| A.常压下五种元素的单质中Z单质的沸点最高 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.W的氢化物的沸点比X的氢化物的沸点高 |
| D.Y元素的非金属性比W元素的非金属性强 |
外围电子构型为4d55s1的元素在周期表中的位置是
| A.第4周期第ⅠB族 | B.第5周期第ⅠB族 |
| C.第4周期第ⅥB族 | D.第5周期第ⅥB族 |
下列各基态原子或离子的电子排布式正确的是
| A.O2-1s22s22p4 | B.Ca [Ar]3d2 |
| C.Fe [Ar]3d54s3 | D.Si 1s22s22p63s23p2 |
以下能级符号错误的是
| A.5s | B.3d | C.3f | D.6p |
a、b、c、d、e五种短周期主族元素,在元素周期表中的相对位置如下表。b与d可以形成两种常见的化合物,下列说法错误的是
| | | a | b | |
| c | | | d | e |
B.原子半径的大小顺序为:a>b>c>d>e
C.b元素在地壳中的含量居第一位
D.元素d的非金属性小于e