下列叙述中正确的是
| A.卤素单质与水反应均可用X2+H2O===HXO+HX表示 |
| B.从F2到I2,卤素单质的颜色随着相对分子质量的增大而加深 |
| C.熔、沸点:Li>Na>K |
| D.还原性:K>Na>Li,故K可以从NaCl溶液中置换出金属钠 |
短周期元素W、X、Y、Z的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同。X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,而Z不能形成双原子分子。根据以上叙述,下列说法中正确的是
| A.上述四种元素的原子半径大小为W<X<Y<Z |
| B.W与Y可形成既含极性共价键又含非极性共价键的化合物 |
| C.W、X、Y、Z原子的核外最外层电子数的总和为20 |
| D.由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 |
下列各组中两种微粒所含电子数不相等的是
| A.H3O+和OH- | B.CO和N2 | C.HNO2和NO2- | D.CH3+和NH4+ |
今年是门捷列夫诞辰180周年。下列事实不能用元素周期律解释的只有
| A.碱性:KOH>NaOH | B.相对分子质量:Ar>K |
| C.酸性:HClO4>H2SO4 | D.元素的金属性:Mg>Al |
“玉兔”号月球车用 Pu作为热源材料。下列关于
Pu作为热源材料。下列关于 Pu的说法正确的是
Pu的说法正确的是
A. Pu与 Pu与 U互为同位素 U互为同位素 | B. Pu与 Pu与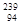 Pu互为同素异形体 Pu互为同素异形体 |
C. Pu与 Pu与 U具有完全相同的化学性质 U具有完全相同的化学性质 | D. Pu与 Pu与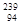 Pu具有相同的最外层电子数 Pu具有相同的最外层电子数 |
根据原子结构及元素周期律的知识,下列推断正确的是
| A.同主族元素含氧酸的酸性随核电荷数的增加而减弱 |
| B.核外电子排布相同的微粒化学性质也相同 |
| C.Cl?、S2?、Ca2+、K+半径逐渐减小 |
D.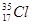 与 与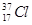 得电子能力相同 得电子能力相同 |
短周期主族元素X、Y、Z、W的原子序数依次增大。X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族。下列说法正确的是
| A.原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) |
| B.Y分别与Z、W形成的化合物中化学键类型相同 |
| C.X的最高价氧化物对应水化物的酸性比W的弱 |
| D.Y的气态简单氢化物的热稳定性比W的强 |
下列有关物质性质的说法错误的是
| A.热稳定性:HCl> HI | B.原子半径:Na> Mg |
| C.酸性:H2SO3>H2SO4。 | D.结合质子能力:S2-> Cl- |
甲~辛等元素在周期表中的相对位置如下表。甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素。下列判断正确的是( )
| A.金属性:甲>乙>丁 |
| B.原子半径:辛>己>戊 |
| C.丙和庚的原子核外电子数相差13 |
| D.乙的单质在空气中燃烧生成只含离子键的化合物 |
下列各组顺序的排列不正确的是
| A.原子半径:Na>Mg>Al | B.热稳定性:HCl> H2S>PH3 |
| C.还原性:I–<Br–<Cl– | D.熔点:金刚石>食盐>干冰 |