有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数)。下列说法正确的是
| A.若X(OH)n为强碱,则Y(OH)n也一定为强碱 |
| B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性 |
| C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2 |
| D.若Y的最高正价为+m,则X的最高正价一定为+m |
已知同周期X、Y、Z三种元素的最高价氧化物对应水化物酸性由强到弱的顺序为:
HXO4>H2YO4>H3ZO4,则下列判断中正确的是
| A.元素非金属性按X、Y、Z的顺序减弱 |
| B.原子的电子能力按X、Y、Z的顺序增强 |
| C.气态氢化物的稳定性按X、Y、Z的顺序增强 |
| D.单质的氧化性按X、Y、Z的顺序增强 |
CCTV-1《焦点访谈》栏目中曾报道“铊中毒事件”,铊再次成为公众关注的焦点。铊的相关信息如下图所示,其中“6s26p1”表示铊原子有6个电子层,最外层有3个电子。下列有关卡片信息解读不正确的是 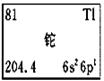
| A.铊的元素符号为Tl | B.铊原子的中子数为204 |
| C.铊位于第六周期ⅢA族 | D.铊的金属性比铝的金属性强 |
若某ⅡB族元素原子序数为x,那么原子序数为x+1的元素位于
| A.ⅢA族 | B.ⅢB族 | C.ⅠB族 | D.ⅠA族 |
X元素的阳离子与Y的阴离子具有相同的核外电子排布,则下列比较中正确的是
| A.原子序数: X<Y | B.原子半径:X<Y |
| C.离子半径:X>Y | D.原子最外层电子数:X<Y |
元素的性质随着元素原子序数的递增而呈周期性变化的原因是
| A.元素原子的核外电子排布呈周期性变化 |
| B.元素的原子半径呈周期性变化 |
| C.元素的化合价呈周期性变化 |
| D.元素的金属性、非金属性呈周期性变化 |
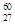 Co是r射线的放射源,关于
Co是r射线的放射源,关于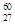 27Co的说法正确的是
27Co的说法正确的是
| A.质子数为 33 | B.中子数为27 | C.质量数为60 | D.核电荷数为60 |
元素周期表中某区域的一些元素多用于制造半导体材料,它们是
| A.左、下方区域的金属元素 | B.金属元素和非金属元素分界线附近的元素 |
| C.右、上方区域的非金属元素 | D.稀有气体元素 |