下列化学用语中,不正确的是
A.氯原子结构示意图:  | B.HCl的电子式: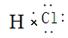 |
| C.H2O分子的结构式:H-O-H | D.乙炔的比例模型: 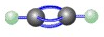 |
对元素周期表和元素周期律的发现有突出贡献的科学家是
| A.拉瓦锡 | B.阿伏加德罗 | C.门捷列夫 | D.道尔顿 |
W、X、Y、Z是短周期元素,其部分性质如表,下列说法正确的是
| W | 单质是淡黄色固体 |
| X | 在地壳中的含量居第二位 |
| Y | 原子最外层电子数是电子总数的2/3 |
| Z | 第三周期原子半径最小的金属 |
A.气态氢化物的热稳定性:X<W
B.最高价氧化物对应水化物的酸性:Y>X
C.离子半径:Z>W
D.Y的氧化物中含有非极性共价键
下列说法不正确的是
| A.钾的金属性比钠强 |
| B.溴的非金属性比氯强 |
| C.VIIA族中原子半径最小的是氟 |
| D.第三周期中,除稀有气体元素外原子半径最大的是钠 |
碘131是碘元素的一种放射性核素。下列关于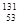 I的说法正确的是
I的说法正确的是
| A.质量数为131 | B.质子数为78 | C.核外电子数为78 | D.中子数为53 |
如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法正确的是( )
| A.X、Y、Z三种元素最低价氢化物的沸点依次升高 |
| B.由X、Y和氢三种元素形成的化合物中只有共价键 |
| C.物质WY2、W3X4、WZ4均有熔点高、硬度大的特性 |
| D.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
短周期主族元素X、Y、Z、W的原子序数依次增大。X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族。下列说法正确的是( )
| A.原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) |
| B.Y分别与Z、W形成的化合物中化学键类型相同 |
| C.X的最高价氧化物对应水化物的酸性比W的弱 |
| D.Y的气态简单氢化物的热稳定性比W的强 |
现有四种元素的基态原子的电子排布式如下:① [Ne]3s23p4;②1s22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是( )
| A.最高正化合价:③>②>① | B.第一电离能:③>②>① |
| C.电负性:③>②>① | D.原子半径:③>②>① |
应用元素周期律和元素周期表,判断下列说法正确的是( )
| A.碱金属单质的熔点随原子序数的增大而降低 |
| B.砹(At)是VIIA族元素,HAt的稳定性大于HCl |
| C.第2周期非金属的气态氢化物溶于水后所得溶液均为酸性 |
| D.铊(TI)与铝同主族,其单质既能与盐酸反应又能与NaOH溶液反应 |
甲、乙两种非金属:①甲比乙容易与氢气化合;②甲能与乙的阴离子发生置换反应;③甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强;④与某金属反应时,甲原子得电子数目比乙的多;⑤甲的单质熔、沸点比乙的低。能说明甲比乙的非金属性强的是( )
| A.只有④ | B.只有⑤ | C.①②③ | D.①②③④⑤ |