亚硝酸钠是一种工业用盐,广泛用于物质合成、金属表面处理等,它的一些性质或用途见图。下列说法不正确的是( )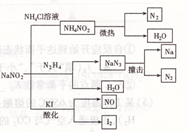
| A.NaNO2的稳定性大于NH4NO2 |
| B.NaNO2与N2 H4反应,NaNO2是氧化剂 |
| C.可用淀粉碘化钾试纸和食醋鉴别NaCl与NaNO2 |
| D.NaN3分解,每产生1molN2转移6mole- |
下列是有关物质的性质或用途的说法中正确的是
① 氯气具有漂白性,可以直接使有色布条褪色;② 二氧化硫具有较强的还原性,不能用浓硫酸干燥;③ SiO2是酸性氧化物,能与氢氟酸反应;④ Al(OH)3是两性氢氧化物,能溶于强酸或强碱。
| A.①②③ | B.②③④ | C.③④ | D.①②④ |
某化学小组用下图所示装置制取氯气,下列说法不正确的是
| A.该装置图中至少存在两处明显错误 |
| B.烧瓶中的MnO2可换成KMnO4 |
| C.在乙后连一盛有饱和食盐水的烧杯可进行尾气处理 |
| D.在集气瓶的导管口处放一片湿润的淀粉碘化钾试纸可以证明是否有氯气逸出 |
如图所示,若向盛有溶液①和溶液②的试管中,通入过量气体X,最终①、②均有沉淀生成的是
| 选项 | X | ①溶液 | ②溶液 |
| A | Cl2 | Na2SO3 | Na2S |
| B | SO2 | Na2SiO3 | Ba(NO3)2 |
| C | NH3 | AgNO3 | AlCl3 |
| D | HCl | CuSO4 | NaAlO2 |
某兴趣小组的同学为探究浓硫酸的吸水性设计了如下实验,理论上能达到实验目的的是
| A.①③ | B.①②③④ | C.①③④ | D.②④ |
能证明碳酸比硅酸酸性强的实验事实是
| A.H2CO3比H2SiO3受热易分解 |
B.高温下能发生反应Na2CO3+SiO2 Na2SiO3+CO2↑ Na2SiO3+CO2↑ |
| C.CO2能溶于水生成碳酸,而SiO2却不溶于水 |
| D.CO2通入Na2SiO3溶液中有胶状沉淀生成 |
在8.08g铁与铜的混和物中,加入200mL 0.6mol/L的稀硝酸,充分反应后剩余金属5.44g。再向其中加入50mL 0.4mol/L的稀硫酸,充分振荡后剩余金属4.48g。若硝酸的还原产物只有NO,下列说法正确的是
| A.剩余的5.44g金属为铁 | B.剩余5.44g金属为铜 |
| C.共生成NO气体 0.03mol | D.8.08g金属中铁的质量分数为0.208 |
加入少许下列一种物质,不能使溴水颜色变浅的是
| A.Mg粉 | B.H2S(g) | C.KI(s) | D.CCl4 |
向FeCl3和BaCl2的混合液中通入过量SO2,有白色沉淀产生。下列说法正确的是
| A.白色沉淀为BaSO3 | B.该实验表明FeCl3有还原性 |
| C.反应后溶液酸性增强 | D.反应后滴加KSCN溶液显红色 |
下图所示的是验证二氧化硫性质的微型实验,a、b、c、d是浸有相关溶液的棉球。将硫酸滴入装有亚硫酸钠固体的培养皿。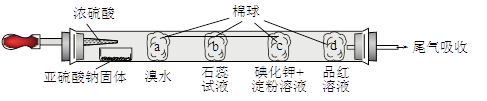
关于此实验的“现象”、“解释或结论”以及对应关系均正确的是
| 选项 | 现象 | 解释或结论 |
| A | a处黄色褪去 | 非金属性:Br>S |
| B | b处变为红色 | 二氧化硫与水反应生成酸性物质 |
| C | c处变为蓝色 | 二氧化硫具有一定的氧化性 |
| D | d处红色先褪去后恢复 | 二氧化硫具有漂白性且漂白性不稳定 |