题目内容
下列是有关物质的性质或用途的说法中正确的是
① 氯气具有漂白性,可以直接使有色布条褪色;② 二氧化硫具有较强的还原性,不能用浓硫酸干燥;③ SiO2是酸性氧化物,能与氢氟酸反应;④ Al(OH)3是两性氢氧化物,能溶于强酸或强碱。
| A.①②③ | B.②③④ | C.③④ | D.①②④ |
C
解析试题分析:氯气具有强氧化性,但不能使干燥的有色布条腿色,说明氯气没有漂白性,则①错误;二氧化硫具有较强的还原性,因为其中所含硫元素容易由+4价升为+6价,但是浓硫酸不能将其氧化,因为浓硫酸中硫元素为+6价,二者不能发生氧化还原反应,因为硫元素无+5价,所以可用浓硫酸干燥二氧化硫,故②错误;二氧化硅只能与强碱反应生成盐和水,不能与强酸反应生成盐和水,氢氟酸是唯一能溶解二氧化硅的弱酸,故③正确;氢氧化铝既能与NaOH溶液反应生成盐和水,又能与盐酸反应生成盐和水,说明氢氧化铝既有酸性又有碱性,因此氢氧化铝是两性氢氧化物,故④正确;综上所述,只有C选项正确。
考点:考查常见无机物的性质,主要涉及氯气的强氧化性、次氯酸的漂白性、二氧化硫的还原性、浓硫酸的强氧化性和吸水性、二氧化硅的特性、氢氧化铝的两性等。

已知铜与稀硫酸不发生反应,但如果在铜与稀硫酸的混合溶液中加入某种盐,就能发生反应,且有气体、有沉淀产生,则该盐是
| A.FeCl3 | B.Ba(NO3)2 | C.Na2SO4 | D.KCl |
下图是某燃煤发电厂处理废气的装置示意图。装置内发生的主要反应中不含( )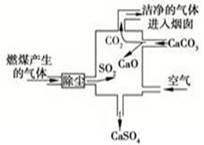
| A.化合反应 | B.分解反应 |
| C.置换反应 | D.氧化还原反应 |
在Fe2(SO4)3、CuSO4、Al2(SO4)3的混合溶液中通入适量H2S,产生的沉淀物是
| A.FeS和CuS | B.CuS | C.CuS和S | D.Al2S3、FeS和CuS |
在8.08g铁与铜的混和物中,加入200mL 0.6mol/L的稀硝酸,充分反应后剩余金属5.44g。再向其中加入50mL 0.4mol/L的稀硫酸,充分振荡后剩余金属4.48g。若硝酸的还原产物只有NO,下列说法正确的是
| A.剩余的5.44g金属为铁 | B.剩余5.44g金属为铜 |
| C.共生成NO气体 0.03mol | D.8.08g金属中铁的质量分数为0.208 |
硝酸铜是制备Cu—Zn—Al系催化剂的重要原料。现有三种制取硝酸铜的实验方案可供选用:①铜与稀硝酸反应制取:3Cu + 8HNO3(稀)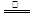 3Cu(NO3)2 + 2NO↑+ 4H2O
3Cu(NO3)2 + 2NO↑+ 4H2O
②铜与浓硝酸反应制取:Cu + 4HNO3(浓)= Cu(NO3)2 + 2NO2↑+ 2H2O
③首先将铜屑在空气中加热生成氧化铜,氧化铜与稀硝酸反应制取:2Cu + O2 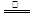 2CuO,CuO + 2HNO3 = Cu(NO3)2 + H2O 下列有关说法正确的是( )
2CuO,CuO + 2HNO3 = Cu(NO3)2 + H2O 下列有关说法正确的是( )
| A.制取等量的硝酸铜,需硝酸的量②最少 |
| B.制取等量的硝酸铜,②产生的有毒气体比①少 |
| C.三种方案中,第③方案最经济环保 |
| D.三种方案的反应都可以在铁质容器中进行 |
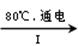 NaClO3溶液
NaClO3溶液 KClO3晶体
KClO3晶体
