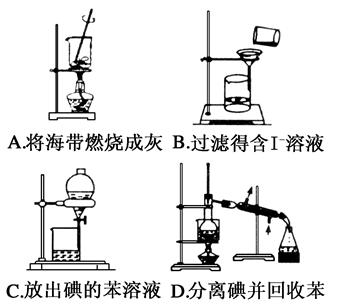
将少量的CO2通入下列溶液中,不能产生沉淀的是( )。
| A.偏铝酸钠溶液 | B.石灰水 | C.氢氧化钡溶液 | D.氯化钙溶液 |
下列有关Cl2的实验操作和装置中,正确的是( )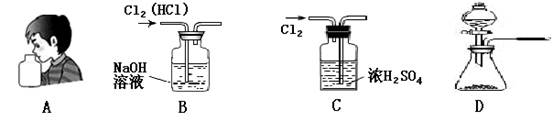
| A.闻Cl2气味 | B.除去Cl2中的HCl |
| C.干燥Cl2 | D.用高锰酸钾和浓盐酸快速制取Cl2 |
根据下图,下列描述不正确的是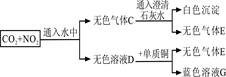
| A.C的成分是气体E与二氧化碳的混和气体 |
| B.浓热的D溶液能把碳单质氧化为二氧化碳 |
| C.气体E遇空气会被氧化成红棕色的气体 |
| D.溶液G是蓝色的硫酸铜溶液 |
下列说法正确的是( )
| A.海水中含量最高的元素是氯 |
| B.海水中含量最高的物质是氯化钠 |
| C.加碘食盐溶液遇淀粉溶液显蓝色 |
| D.加碘食盐中的碘是含碘元素的化合物 |
从海水中可以提取溴,但得到的液溴中常常溶有少量氯气,除去氯气应该采用的方法是( )
| A.加入适量的Na2CO3溶液 |
| B.通入溴蒸气 |
| C.加入适量的NaOH溶液 |
| D.加入适量的NaBr溶液 |
常温下,将Cl2缓慢通入一定量的水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol·L-1的氢氧化钠溶液,整个过程中pH变化如图所示,下列有关叙述正确的是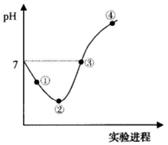
| A.②点之前所发生反应的离子方程式为Cl2+H2O=2H++Cl-+ClO﹣ |
| B.③点所示溶液中:c(Na+)= c(HClO)+2c(ClO-) |
| C.实验进程中溶液的pH可以用pH试纸测得 |
| D.曲线的起始点水的电离程度最大 |
一定温度下,硫酸铜受热分解生成CuO、SO2、SO3和O2。已知:SO2、SO 3都能被碱石灰和氢氧化钠溶液吸收。用下图装置加热硫酸铜粉末直至完全分解。若硫酸铜粉末质量为10.0 g,完全分解后,各装置的质量变化关系如下表所示。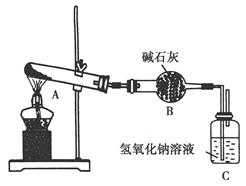
| 装置 | A(试管+粉末) | B | C |
| 反应前 | 42.0 g | 75.0 g | 140.0 g |
| 反应后 | 37.0 g | 79.5 g | 140.0 g |
请通过计算,推断出该实验条件下硫酸铜分解的化学方程式是( )
A.4CuSO4
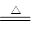 4CuO+2SO3↑+2SO2↑+O2↑
4CuO+2SO3↑+2SO2↑+O2↑B.3CuSO4
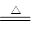 3CuO+SO3↑+2SO2↑+O2↑
3CuO+SO3↑+2SO2↑+O2↑C.5CuSO4
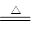 5CuO+SO3↑+4SO2↑+2O2↑
5CuO+SO3↑+4SO2↑+2O2↑D.6CuSO4
 6CuO+4SO3↑+2SO2↑+O2↑
6CuO+4SO3↑+2SO2↑+O2↑