下列叙述正确的是 ( )。
| A.浓硫酸是一种干燥剂,能够干燥氢气、氧气、氨气等气体,但不能干燥有较强还原性的HI、H2S等气体 |
B.浓硫酸与单质硫反应的化学方程式为:S+2H2SO4(浓)  3SO2↑+2H2O,在此反应中,浓硫酸既表现了其强氧化性又表现了其酸性 3SO2↑+2H2O,在此反应中,浓硫酸既表现了其强氧化性又表现了其酸性 |
| C.把足量铜粉投入到只含H2SO4 2 mol的浓硫酸中,得到气体体积标准状况下为22.4 L |
| D.常温下能够用铁、铝等容器盛放浓H2SO4,是因为浓H2SO4的强氧化性使其钝化 |
氯气是一种化学性质很活泼的非金属单质,它具有较强的氧化性,下列叙述中不正确的是 ( )。
| A.红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟 |
| B.通常状况下,干燥的氯气能与Fe反应 |
| C.纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶口呈现雾状;光照H2和Cl2的混合气体时,因迅速化合而爆炸 |
| D.氯气能与水反应生成HClO和HCl,久置氯水最终变为稀盐酸 |
(CN)2、(OCN)2、(SCN)2等物质的性质与卤素单质相似,而CN-、OCN-、SCN-等离子的性质与卤离子相似,化学上分别将其称之为类卤素和类卤离子,不同的卤素也可以生成卤素互化物,如BrF3。下列关于(CN)2的性质的叙述中,不像卤素的是( )
| A.能在空气中燃烧 |
| B.可与银、汞、铅等生成难溶盐 |
| C.在碱溶液中生成CN-和OCN- |
| D.与Cl2反应生成CNCl |
实验室既可用浓盐酸与MnO2在加热时反应制备Cl2,也可用KMnO4与浓盐酸在常温下反应制备Cl2,下列有关说法中不正确的是( )
| A.由题目信息知:KMnO4的氧化性比MnO2的强 |
| B.制备氯气的整个实验过程中,只需要使用氧化剂与还原剂 |
| C.用排气法收集不需要利用其他试剂就能确定集气瓶中已收集满气体 |
| D.用足量MnO2与含有4 mol HCl的浓盐酸在加热条件下反应,得到Cl2的物质的量小于1 mol |
下列是卤素单质(F2、Cl2、Br2、I2)的沸点与相对分子质量的关系图,下列说法错误的是( )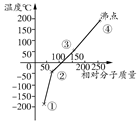
| A.单质①是最活泼的非金属单质 |
| B.单质②能使品红溶液褪色 |
| C.单质③在常温下是液态 |
| D.单质的氧化性强弱顺序是④>③>②>① |
下列实验现象与新制氯水中的某些成分(括号内物质)没有关系的是( )
| A.将NaHCO3固体加入新制氯水中,有无色气泡产生(H+) |
| B.使红色布条褪色(HCl) |
| C.向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发现呈红色(Cl2) |
| D.滴加AgNO3溶液生成白色沉淀(Cl-) |
在氯水中存在着如下反应:Cl2+H2O=HCl+HClO,因此氯水中存在多种分子和离子。在下列实验现象中与相应离子或分子性质关系正确的是( )
| A.氯水有刺激性气味说明氯水中有HCl |
| B.氯水中滴入品红溶液,溶液为无色说明氯水中有Cl2 |
| C.向氯水中通入SO2气体,氯水黄绿色褪去说明Cl2发生了反应 |
| D.向氯水中加入CaCO3有气泡产生,说明有HCl和HClO |
氯气与二氧化硫都有漂白作用,若将等物质的量的这两种气体混合后通入品红和BaCl2的混合溶液中,能观察到的现象是( )
①溶液很快褪色 ②溶液不褪色 ③出现沉淀 ④不出现沉淀
| A.①② | B.①③ | C.②③ | D.②④ |
现有一Na2SO3、Na2SO4混合物样品ag,为了测定其中Na2SO3的质量分数,设计了如下方案,其中明显不合理的是
| A.将样品配制成溶液V1L,取其中25.00mL用标准KMnO4溶液滴定,消耗标准KMnO4溶液V2mL |
| B.向样品中加足量H2O2,再加足量BaCl2溶液,过滤,将沉淀洗涤、干燥,称量其质量为bg |
| C.将样品与足量稀盐酸充分反应后,再加入足量BaCl2溶液,过滤,将沉淀洗涤、干燥,称量其质量为cg |
| D.将样品与足量稀盐酸充分反应,生成的气体依次通过盛有饱和NaHSO3的洗气瓶、盛有浓H2SO4的洗气瓶、盛有碱石灰的干燥管Ⅰ、盛有碱石灰的干燥管Ⅱ,测定干燥管Ⅰ增重dg |
下列事实与浓硫酸具有强氧化性有关的是
①常温时用铁制容器运输浓硫酸
②硫酸工业生产中,用浓硫酸吸收SO3
③浓硫酸使蔗糖炭化变黑并有大量气体产生
④浓硫酸用于生产磷肥
⑤浓硫酸不能用来干燥HBr
| A.①③④ | B.①②③ | C.①③⑤ | D.②③④⑤ |