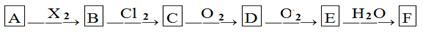海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、SO42-、HCO3-、CO32-等离子,火力发电时排放的烟气可用海水脱硫,其工艺流程如下图所示,下列说法错误的是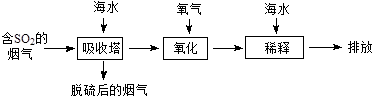
| A.海水pH约为8的原因主要是天然海水含CO32-、HCO3- |
B.吸收塔中发生的反应有SO2+H2O H2SO3 H2SO3 |
| C.氧化主要是氧气将HSO3-、SO32-、H2SO3氧化为SO42- |
| D.经稀释“排放”出的废水中,SO42-浓度与海水相同 |
下列图象描述正确的是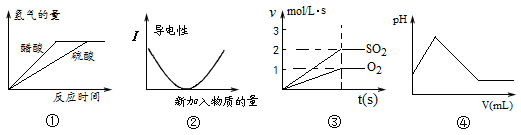
| A.图①表示体积和PH值均相同的稀硫酸和醋酸,和足量的镁反应生成H2量的关系 |
| B.图②表示向氨水中滴加醋酸,溶液导电性变化的关系 |
C.图③表示2SO2(g)+O2(g) 2SO3(g)反应中,SO2和O2反应速率大小关系 2SO3(g)反应中,SO2和O2反应速率大小关系 |
| D.图④表示向H2S中通入Cl2时,溶液的pH大小变化关系 |
已知氨气可以与灼热的氧化铜反应得到氮气和金属铜,用下图中的装置可以实现该反应。
实验时C中粉末逐渐变为红色,D中出现无色液体。下列有关说法正确的是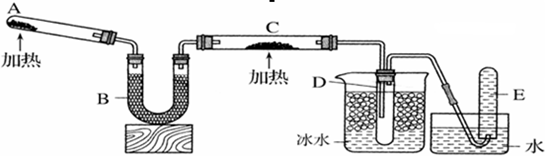
| A.反应中氧化剂和还原剂的物质的量之比为2∶3 |
| B.装置B中加入的物质可以是碱石灰或无水氯化钙 |
| C.装置D中液体可以使干燥的红色石蕊试纸变蓝 |
| D.为防止装置D中发生倒吸,可以改用向下排空气法收集氮气 |
无色的混合气体甲,可能含NO、CO2、NO2、NH3、N2中的几种,将100 mL甲气体经过下图实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为
| A.NH3、NO2、N2(体积比5∶16∶4) |
| B.NH3、NO、CO2(体积比5∶8∶12) |
| C.NH3、NO2、CO2 (体积比3∶8∶4) |
| D.NO、CO2、N2(体积比8∶12∶5) |
下列说法不正确的是
| A.在稀硫酸中加入铜粉,铜粉不溶解,再加入Cu(NO3)2固体,铜粉仍不溶解 |
| B.某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性 |
| C.铜与稀硝酸反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O |
| D.HNO3→NO→NO2,以上各步变化均能通过一步实现 |
下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。已知:2KMnO4+16HCl—→2KCl+5Cl2↑+2MnCl2+8H2O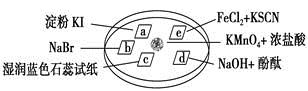
对实验现象的“解释或结论”正确的是
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变红色 | 还原性:Fe2+>Cl- |
将足量的SO2通入下列各溶液中,所含离子还能大量共存的是
| A.K+、SiO32-、Cl-、NO3- |
| B.H+、NH4+、Al3+、SO42- |
| C.Na+、Cl-、MnO4-、SO42- |
| D.Na+、CO32-、CH3COO-、HCO3- |
某浓H2SO4的标签上写明含H2SO4 96~98.3%,欲得其准确的值,有效的方法是
| A.测pH值 | B.测导电性大小 | C.测密度 | D.进行中和滴定 |