题目内容
无色的混合气体甲,可能含NO、CO2、NO2、NH3、N2中的几种,将100 mL甲气体经过下图实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为
| A.NH3、NO2、N2(体积比5∶16∶4) |
| B.NH3、NO、CO2(体积比5∶8∶12) |
| C.NH3、NO2、CO2 (体积比3∶8∶4) |
| D.NO、CO2、N2(体积比8∶12∶5) |
B
解析试题分析:该无色气体通过足量的浓硫酸,时氨气被吸收,由于气体体积减小20ml,则氨气的体积为20ml;再通过足量的Na2O2的干燥管时,气体变为红棕色,则说明原气体中含有NO和CO2。发生反应:2Na2O2+2CO2 =Na2CO3+ O2;O2+2NO=2NO2。当气体通过足量的水时由于得到酸性溶液,而几乎无气体剩余。所以没有N2。发生反应:O2+4NO2+2H2O=4HNO3。或3O2+4NO+2H2O=4HNO3.由上述方程式得关系式为6CO2~3O2~4NO则在剩余的80ml的气体中CO2的体积为80ml×6/10=48ml;NO的体积为80ml×4/10=32ml。因此在原混合气体中含有NH3、NO、CO2。它们的物质的量的比或体积比为20:32:48=5∶8∶12。故选项为B。
考点:考查混合气体中成分的确定及体积比的计算的知识。

卤素间形成的化合物如“IF5、BrCl、IBr”等称为卤素互化物,化学性质与卤素单质类似,则下列关于卤素互化物的性质的描述及发生的相关反应不正确的是
| A.IF5 + 3H2O = HIO3 +5HF |
| B.3IBr +2Fe = FeI3 + FeBr3 |
| C.BrCl的氧化性强于I2 |
| D.IBr可以与NaOH溶液反应生成2种盐 |
一定量的浓硝酸与过量的铜充分反应,生成的气体是
| A.只有NO2 | B.只有NO | C.NO2和NO | D.NO2和H2 |
某浓H2SO4的标签上写明含H2SO4 96~98.3%,欲得其准确的值,有效的方法是
| A.测pH值 | B.测导电性大小 | C.测密度 | D.进行中和滴定 |
常温常压下,两个容积相同的烧瓶中分别盛满X和Y两种气体,打开开关a,使两烧瓶内的气体相通,最后容器内的压强由大到小的顺序排列正确的是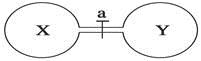
| 编号 | ① | ② | ③ | ④ |
| 气体X | HI | NH3 | H2 | NO |
| 气体Y | Cl2 | HCl | Cl2 | O2 |
A.②>③>①>④ B.③>①=④>②
C.③>①>④>② D.④>①>②>③
下列气体:①NH3 ②NO2 ③NO ④O2 ⑤SO2中,适于用下图装置制取和收集的气体是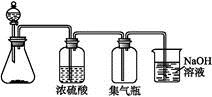
| A.①② | B.②③ | C.③④ | D.②⑤ |
用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是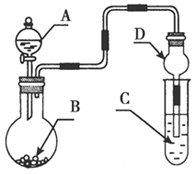
| A.若A为浓盐酸,B为KMnO4晶体,C中盛有紫色石蕊溶液,则C中溶液最终呈红色 |
| B.实验仪器D可以起到防止溶液倒吸的作用 |
| C.若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,则C中溶液先产生白色沉淀后沉淀又溶解 |
| D.若A为浓H2SO4,B为Cu,C中盛有澄清石灰水,则C中溶液变浑浊 |
NaCl是一种化工原料,可以制备一系列物质,如图所示。下列说法正确的是( )。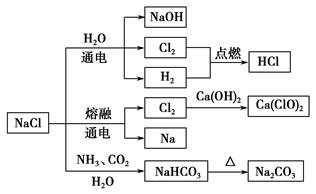
| A.25 ℃时,NaHCO3在水中的溶解度比Na2CO3的大 |
| B.石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 |
| C.常温下干燥的Cl2能用钢瓶贮运,所以Cl2不与铁反应 |
| D.图示转化反应都是氧化还原反应 |