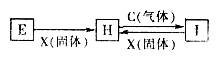下列有关说法正确的是( )
| A.大多数金属在自然界以游离态形式存在 |
| B.工业上,一般用热还原法获得Hg和Ag |
| C.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 |
| D.人们常用钢作建造材料而不用纯铁主要原因是钢的机械性能更好 |
甲、乙、丙、丁为中学常见物质,其中甲、乙为单质,丙为氧化物,它们之间存在如图所示的转化关系。 下列说法正确的是
下列说法正确的是
| A.若甲、乙均为金属单质,则丁所属的物质类别一定是碱性氧化物 |
| B.若甲为金属单质,乙为非金属单质,则甲只能是Mg |
| C.若甲、乙元素是同主族元素,根据元素周期表推测,此时乙单质可能是Si |
| D.若甲、乙元素是同周期元素,则该反应的化学方程式一定为:2F2 + 2H2O=4HF + O2 |
下列说法错误的是;
| A.某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为水中溶解了较多的CO2 |
| B.硅酸盐NaAlSiO4·nH2O可改写成氧化物形式为:Na2O·Al2O3·2SiO2·2nH2O |
| C.Al65Cu23Fe12是一种拟晶,具有合金的优良物理性能,其硬度比金属Al、Cu、Fe都大 |
| D.过量铁与浓硫酸加热反应可以得到氢气 |
下列解释实验事实的化学方程式正确的是
| A.5molFe和4molCl2反应:5Cl2+4Fe点燃2FeCl2+2FeCl3 |
| B.2molKMnO4和3molH2O2在酸性条件下反应:2MnO4-+3H2O2+6H+=Mn2++4O2↑+6H2O |
| C.在电解液为氢氧化钾的甲醇燃料电池内电路中,阳极的电极反应式为:CH3OH-6e-+8OH-=CO32-+6H2O |
| D.向NaAlO2溶液中通入过量CO2:CO2+3H2O+2AlO2-=2Al(OH)3↓+CO32- |
现代工业常以氯化钠、二氧化碳和氨气为原料制备纯碱,部分工艺流程如下:
有关说法错误的是
| A.反应Ⅰ原理为CO2 + NH3 + NaCl + H2O → NaHCO3↓ + NH4Cl |
| B.向饱和NaCl溶液中先通入足量的CO2,再通入足量的NH3 |
| C.反应Ⅰ生成的沉淀,经过过滤、洗涤、煅烧可得到纯碱 |
| D.往母液中通入氨气,加入细小的食盐颗粒并降温,可使氯化铵析出 |
有4种金属a、b、c、d,它们与浓HNO3反应时,只有a不反应;往这4种金属粉末的混合物中加入盐酸,其中b、c溶解,过滤后,在滤液中加入过量的NaOH溶液,可得到c离子的沉淀,则这4种金属的活动性强弱的顺序可能是
| A.c > b > d > a | B.b > a > d > c | C.a > b > c > d | D.d > c > b > a |
下列物质都具有漂白作用,其中漂白原理没有利用物质化学性质的是
| A.过氧化钠 | B.二氧化硫 | C.次氯酸 | D.活性炭 |
下列说法正确的是
| A.汽油、柴油、植物油都属烃类物质且均为纯净物 |
| B.单质硅常用于制造芯片和光导纤维 |
| C.等质量的气态乙醇和液态乙醇分别完全燃烧,前者放出的热量更多 |
| D.漂白精和明矾都常用于自来水的处理,二者作用原理相同 |