臭氧可使湿润的淀粉KI试纸变蓝,化学方程式为2KI+O3+H2O=2KOH+I2+O2。下列叙述中正确的是( )
| A.在反应中水被氧化成氧气 | B.该反应中水是氧化剂 |
| C.每生成1 mol I2,转移的电子数为1 mol | D.反应中氧化剂与还原剂的物质的量之比为1∶2 |
下列反应类型的判断,不正确的是( )
A.CO2+H2O H2CO3化合反应 H2CO3化合反应 |
B.Cu(OH)2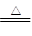 CuO+H2O 分解反应 CuO+H2O 分解反应 |
C.MnO2+2CO Mn+2CO2置换反应 Mn+2CO2置换反应 |
| D.NaCl+AgNO3=AgCl↓+NaNO3复分解反应 |
下列转化,需要加入氧化剂才能完成的是
| A.H+ →H2 | B.MnO4-→Mn2+ | C.CO2→CO32- | D.S2-→SO42- |
下列反应中氯元素仅被还原的是
| A.5Cl2+I2+6H2O=10HCl+2HIO3 |
| B.2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O |
C.MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑ MnCl2+2H2O+Cl2↑ |
| D.HCl+NaOH=NaCl+H2O |
已知常温下在溶液中可发生如下两个离子反应:
Ge4++Fe2+=Fe3++Ge3+①;Sn2++2Fe3+=2Fe2++Sn4+②
由此可以确定Fe2+、Ge3+、Sn2+三种离子的还原性由强到弱的顺序是
| A.Sn2+、Fe2+、Ge3+ | B.Sn2+、Ge3+、Fe2+ |
| C.Ge3+、Fe2+、Sn2+ | D.Fe2+、Sn2+、Ge3+ |
此反应:MnO2 +4 HCl(浓)  MnCl2 +Cl2↑+2H2 O,氧化剂和还原剂的物质的量比为
MnCl2 +Cl2↑+2H2 O,氧化剂和还原剂的物质的量比为
| A.4∶1 | B.1∶4 | C.1∶1 | D.1∶2 |
需要加入适当的氧化剂才能实现的反应
| A.PCl3→PCl5 | B.MnO4-→Mn2+ | C.SO3→SO42- | D.CO2→CO32- |
氧化还原反应实际上包含氧化和还原两个过程。(1)向氯酸钠的酸性水溶液中通入二氧化硫,该反应中氧化过程的反应式为:SO2+2H2O – 2e-→ SO42- + 4H+; (2)向亚氯酸钠(NaClO2)固体中通入用空气稀释的氯 气,该反应中还原过程的反应式为:Cl2 + 2e-→ 2Cl-。在(1)和(2)反应中均会生成产物X,则X的化学式为( )
| A.NaClO | B.NaClO4 | C.HClO | D.ClO2 |
从海水中提取溴有如下反应:5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O。与上述反应在氧化还原原理上最相似的是( )
| A.2NaBr+Cl2=2NaCl+Br2 |
| B.AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl |
| C.2H2S+SO2=2H2O+3S |
| D.2FeCl3+H2S=2FeCl2+S↓+2HCl |
过氧化氢(O为—1价)在二氧化锰催化作用下分解放出氧气的反应机理如下:
①MnO2 + H2O2 + 2H+ = Mn2+ + O2↑ + 2H2O ②Mn2+ + H2O2 = MnO2 + 2H+
下列说法正确的是( )
| A.H2O2在①中是氧化剂,在②中是还原剂 |
| B.在①中每生成1 mol O2,转移的电子数为1.204×1024 |
| C.Mn2+在①中是还原产物,在②中是氧化产物 |
| D.在二氧化锰催化作用下,1 mol H2O2分解生成22.4 L O2 |