某元素在化学反应中,由化合态变成游离态,则下列说法中正确的是( )
①该元素一定被氧化 ②该元素一定被还原 ③该元素可能被氧化,也可能被还原 ④元素化合价降为0 ⑤生成的单质为氧化产物 ⑥生成的单质为还原产物 ⑦生成的单质既可能为氧化产物也可能为还原产物 ⑧该过程不一定非得加氧化剂或还原剂才能实现 ⑨该反应不一定是放热反应 ⑩该反应一定不是复分解反应
| A.③⑦⑧⑨⑩ | B.①⑤⑩ | C.②④⑥⑩ | D.①②④⑤⑥ |
将18 g铜和铁的混合物投入200 mL稀硝酸中,充分反应后得到标准状况下2.24 L NO,剩余9.6 g金属;继续加入200 mL等浓度的稀硝酸,金属完全溶解,又得到标准状况下2.24 L NO。若向反应后的溶液中加入KSCN溶液,溶液不变红,则下列说法中正确的是( )
| A.原混合物中铜和铁各0.15 mol |
| B.稀硝酸的物质的量浓度为1 mol·L-1 |
| C.第一次剩余9.6 g金属为铜和铁 |
| D.再加入上述200 mL稀硝酸,还会得到标准状况下2.24 L NO |
新型纳米材料MFe2Ox(3<x<4)中M表示+2价的金属元素,在反应中化合价不发生变化。常温下,MFe2Ox能使工业废气中的SO2转化为S,流程如下:
则下列判断正确的是( )
| A.MFe2Ox是还原剂 |
| B.SO2是该反应的催化剂 |
| C.x>y |
| D.SO2发生了置换反应 |
已知离子方程式:As2S3+H2O+NO3—―→AsO43—+SO42—+NO↑+______K(未配平),下列说法错误的是( )。
| A.配平后水的化学计量数为4 |
| B.反应后溶液呈酸性 |
| C.配平后氧化剂与还原剂的物质的量之比为3∶28 |
| D.氧化产物为AsO43—和SO42— |
氯酸是一种强酸,浓度超过40%时会发生分解,该反应可表示为aHClO3―→bO2↑+cCl2↑+dHClO4+eH2O,下列有关说法不正确的是 ( )。
| A.由反应可确定氧化性:HClO3>O2 |
| B.由非金属性:Cl>S,可推知酸性:HClO3>H2SO4 |
| C.若氯酸分解所得1 mol混合气体的质量为45 g,则反应的化学方程式可表示为3HClO3===2O2↑+Cl2↑+HClO4+H2O |
| D.若化学计量数a=8,b=3,则生成3 mol O2时该反应转移20 mol电子 |
硫氰(SCN)2的化学性质和卤素(X2)类似,称为拟卤素,如(SCN)2+H2O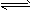 HSCN+HSCNO,它们阴离子的还原性强弱为Cl-<Br-<SCN-<I-,下列说法不正确的是( )
HSCN+HSCNO,它们阴离子的还原性强弱为Cl-<Br-<SCN-<I-,下列说法不正确的是( )
| A.Cl2可以与KSCN溶液反应 |
| B.(SCN)2可以与KI溶液反应 |
| C.KSCN溶液可以与FeCl3溶液反应 |
| D.(SCN)2可以与KBr溶液反应 |
锰酸钾可用于油脂、纤维、皮革的漂白等,其可由KOH、KClO3和MnO2经共熔制备,反应原理为6KOH+KClO3+3MnO2 KCl+3K2MnO4+3H2O。下列有关说法中正确的是 ( )。
KCl+3K2MnO4+3H2O。下列有关说法中正确的是 ( )。
| A.KOH和KCl中均含有共价键 |
| B.MnO2在反应中被还原 |
| C.K2MnO4的氧化性大于KClO3 |
| D.该反应中,每生成3 mol K2MnO4转移的电子数为6×6.02×1023 |
有如下变化:A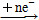 An- ΔH1<0,B
An- ΔH1<0,B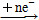 Bn- ΔH2<0,且ΔH1<ΔH2。下列说法中正确的是( )。
Bn- ΔH2<0,且ΔH1<ΔH2。下列说法中正确的是( )。
| A.氧化性:A<B | B.还原性:An-<Bn- |
| C.稳定性:B<A | D.稳定性:An-<Bn- |
下列说法正确的是( )。
| A.反应Na→Na2O→Na2O2中钠元素被连续氧化 |
| B.1 mol金属钠发生反应Na→Na2O和发生反应Na→Na2O2转移电子数相等 |
| C.1 mol Cl2与足量Fe反应转移3 mol电子 |
| D.将1 mol Cl2通入1 L水中转移的电子为1 mol |
向酸化过的MnSO4溶液中滴加(NH4)2S2O8(过二硫酸铵)溶液会发生反应:Mn2++S2O82—+H2O―→MnO4—+SO42—+H+。下列说法不正确的是 ( )。
| A.可以利用该反应检验Mn2+ |
| B.氧化性比较:S2O82—>MnO4— |
| C.MnSO4溶液可以使用盐酸酸化 |
| D.若有0.1 mol氧化产物生成,则转移电子0.5 mol |