根据表中信息,判断下列叙述中正确的是( )
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | | FeBr2 | / | | Cl- |
| ② | KClO3 | 浓盐酸 | / | Cl2 | |
| ③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
A.表中①组的反应可能有一种或两种元素被氧化
B.氧化性强弱的比较:KClO3>Fe3+>Cl2>Br2
C.表中②组反应的还原产物是KCl,电子转移数目是6NA
D.表中③组反应的离子方程式为:2MnO4—+3H2O2+6H+
 2Mn2++4O2↑+6H2O
2Mn2++4O2↑+6H2O 有下列三个反应:
①Cl2+FeI2 FeCl2+I2
FeCl2+I2
②2Fe2++Br2 2Fe3++2Br-
2Fe3++2Br-
③Co2O3+6HCl 2CoCl2+Cl2↑+3H2O,
2CoCl2+Cl2↑+3H2O,
下列说法中正确的是( )
| A.①②③中氧化产物分别是FeCl2、Fe3+、Cl2 |
| B.根据以上方程式可以得到氧化性Cl2>Co2O3>Fe3+ |
| C.在反应③中生成1 mol Cl2时,有2 mol HCl被氧化 |
D.根据反应①②一定可以推理得到Cl2+FeBr2 FeCl2+Br2 FeCl2+Br2 |
从矿物学资料查得,一定条件下自然界存在如下反应:
14CuSO4+5FeS2+12H2O = 7X+5FeSO4+12H2SO4,下列说法正确的是 ( )
| A.X的化学式为CuS,它既是氧化产物又是还原产物 |
| B.5 mol FeS2发生反应,有10 mol电子转移 |
| C.产物中的SO42-离子有一部分是氧化产物 |
| D.FeS2只作还原剂 |
现榨的苹果汁在空气中会由淡绿色变为棕黄色,其原因可能是( )
| A.苹果汁中含有Cu2+ | B.苹果汁中的Fe2+变成Fe3+ |
| C.苹果汁含有OH- | D.苹果汁含有Na+ |
液态金属汞常温下即可蒸发,其蒸气有剧毒, 实验室为监测空气中汞蒸气的含量,通常悬挂有CuI的滤纸,根据滤纸是否变色或颜色发生变化的时间来判断空气中汞的含量,其反应为:
4CuI+Hg= Cu2HgI4+2Cu(I的化合价反应前后均为-1价的)。下列有关说法不正确的是( )
| A.上述反应的产物Cu2HgI4中,Hg的化合价为+2 |
| B.上述反应中氧化剂是CuI |
| C.上述反应中Cu元素仅有一半被还原 |
| D.上述反应中生成64gCu时,转移的电子数为2NA |
向酸化过的MnSO4溶液中滴加(NH4)2S2O8(过二硫酸铵)溶液会发生反应:Mn2++S2O82-+H2O―→MnO4-+H++SO42-。下列说法不正确的是( )
| A.可以利用该反应检验Mn2+ |
| B.氧化性比较:S2O82->MnO4- |
| C.MnSO4溶液可以使用盐酸酸化 |
| D.若有0.1 mol氧化产物生成,则转移电子0.5 mol |
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对生态系统造成很大的损害,其中还原沉淀法是常用的一种处理方法。流程如下:
其中第①步中存在平衡:2CrO42- (黄色)+2H+??Cr2O72- (橙色)+H2O。下列有关说法正确的是( )
| A.第①步当2v(Cr2O72-)=v(CrO42-)时,达到了平衡状态 |
| B.对于上述平衡,加入适量稀硫酸后,溶液颜色变黄色,则有利于CrO42-的生成 |
| C.第②步中,还原0.1 mol Cr2O72-需要45.6 g FeSO4 |
| D.第③步沉淀剂a可以使用NaOH等碱性物质 |
将一定量的Fe和Fe2O3的混合物放入250 mL、1.8 mol·L-1的HNO3溶液中,当固体混合物完全溶解后,在标准状况下生成1.12 L NO(HNO3的还原产物仅此一种),再向反应后的溶液中加入1.0 mol·L-1 NaOH溶液,若要使铁元素完全沉淀,所加入的NaOH溶液的体积最少应为( )
| A.300 mL | B.400 mL | C.450 mL | D.500 mL |
已知NaCN溶液呈碱性,(CN)2与卤素单质的性质相似,CN-的还原性介于Br-、I-之间。下列变化不能发生的是( )
A.HCN H++CN- H++CN- |
| B.(CN)2+CH2=CH2―→NC—CH2—CH2—CN |
| C.(CN)2+2Br-=2CN-+Br2 |
| D.(CN)2+2OH-=CN-+CNO-+H2O |
 aTiCl4+cCO反应(1)
aTiCl4+cCO反应(1)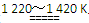 Ti+2MgCl2反应(2)
Ti+2MgCl2反应(2)