下列反应属于氧化还原反应,但水既没有做氧化剂又没有做还原剂的是
| A.2F2+2H2O ="4HF" +O2 |
| B.Na2O+H2O=2NaOH |
| C.Cl2+H2O =2HCl+HClO |
| D.CaO+H2O =Ca(OH)2 |
已知某溶液中Cl-、Br-、I-的物质的量之比为2∶3∶4,现欲使溶液中的Cl-、Br-、I-的物质的量之比改变成4∶3∶2,那么要通入Cl2的物质的量是原溶液中I-的物质的量的 ( )。
A.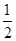 | B.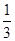 | C.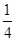 | D.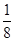 |
氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:aHClO3=bO2↑+cCl2↑+dHClO4+eH2O,下列说法正确的是( )
| A.由反应可知,氧气、氯气均为氧化产物 |
| B.若化学计量数a=8,则该反应转移电子数为12e- |
| C.若b确定,则方程式中其他物质的化学计量数均能确定 |
| D.若氯酸分解所得混合气体,1 mol混合气体质量为51.5 g,则反应方程式可表示为:5HClO3=O2↑+Cl2↑+3HClO4+H2O |
将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:
①SO2+2Fe3++2H2O=SO42-+2Fe2++4H+
②Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
下列有关说法不正确的是( )
| A.氧化性Cr2O72->Fe3+>SO2 |
| B.Cr2O72-能将Na2SO3氧化成Na2SO4 |
| C.若33.6 L SO2(标准状况)参加反应,则最终消耗K2Cr2O7 0.5 mol |
| D.反应中Fe2(SO4)3既是氧化剂,又是还原剂 |
Na2FeO4是一种高效多功能水处理剂。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,下列说法中不正确的是( )
| A.Na2O2在上述反应中只作氧化剂 |
| B.Na2FeO4既是氧化产物又是还原产物 |
| C.Na2FeO4处理水时,既能杀菌,又能在处理水时产生胶体净水 |
| D.2 mol FeSO4发生反应时,共有10 mol电子发生转移 |
被称为万能还原剂的NaBH4溶于水并和水反应:NaBH4+2H2O=NaBO2+4H2↑,下列说法中正确的是(NaBH4中H为-1价)( )
| A.NaBH4既是氧化剂又是还原剂 |
| B.NaBH4是氧化剂,H2O是还原剂 |
| C.硼元素被氧化,氢元素被还原 |
| D.被氧化的元素与被还原的元素质量之比为1:1 |
古代曾用绿矾加强热得到硫酸、红色粉末和有刺激性气味的气体,此反应属于( )
| A.有氧化还原的分解反应 |
| B.无氧化还原的分解反应 |
| C.只是氧化还原反应 |
| D.只是分解反应 |
下列氧化还原反应中,实际参加反应的氧化剂与还原剂的物质的量之比正确的是( )
①KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O;1:6
②Fe2O3+2Al Al2O3+2Fe;1:2
Al2O3+2Fe;1:2
③SiO2+3C=SiC+2CO↑;1:2
④3NO2+H2O=2HNO3+NO;2:1
| A.①③ | B.②③ | C.②④ | D.①④ |
根据以下实验事实,判断选项中四种微粒在酸性条件下,氧化性由强到弱的顺序是( )
(1)向FeCl3溶液中滴加KI溶液,再加入CCl4振荡,CCl4层呈紫红色;
(2)向FeCl2溶液中加入氯水,再加入KSCN溶液,溶液呈红色;
(3)向KMnO4溶液中加入浓盐酸,振荡后紫色褪去。
| A.I2>Cl2>Fe3+>MnO4- |
| B.MnO4->Cl2>Fe3+>I2 |
| C.Cl2>I2>Fe3+,MnO4->Fe3+ |
| D.Fe3+>MnO4->Cl2>I2 |
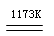 aTiCl4+cCO……反应①
aTiCl4+cCO……反应① Ti+2MgCl2……反应②
Ti+2MgCl2……反应②