在热的稀硫酸溶液中溶解11.4g FeSO4。当加入50mL 0.50mol/L KNO3溶液后,使其中的Fe2+全部转化为Fe3+。KNO3溶液也完全反应,并有NxOy气体逸出,此NxOy气体为
| A.N2O | B.N2O3 | C.NO2 | D.NO |
在真空密闭装置中,亚氯酸钠(NaClO2)固体在一定条件下发生分解反应,从物质组成的角度看,不可能生成的产物是
| A.NaCl和O2 | B.NaClO3和NaClO |
| C.NaClO3和Cl2 | D.NaClO3和NaCl |
在反应Cu+2 H2SO4(浓)  CuSO4+SO2↑+2H2O中,还原剂是
CuSO4+SO2↑+2H2O中,还原剂是
| A.C u | B.H2SO4 | C.CuSO4 | D.SO2 |
已知:将Cl2通人适量KOH溶液,产物中可能有KC1、KClO、KC1O3,且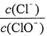 的值与温度高低有关。当n(KOH)=amol时,下列有关说法错误的是( )
的值与温度高低有关。当n(KOH)=amol时,下列有关说法错误的是( )
A.若某温度下,反应后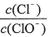 =11,则溶液中 =11,则溶液中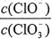 = =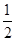 |
| B.参加反应的氯气的物质的量等于0.5amol |
C.改变温度,反应中转移电子的物质的量ne的范围: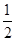 amol≤ne≤ amol≤ne≤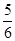 amol amol |
D.改变温度,产物中KC1O3的最大理论产量为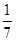 amol amol |
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3 = K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75mol,则下列判断正确的是( )
| A.生成40.0LN2(标准状况) | B.有0.250molKNO3被氧化 |
| C.转移电子的物质的量为2.5mol | D.被氧化的N原子的物质的量为3.75mol |
已知氧化性Br2>Fe3+。FeBr2溶液中通入一定量的Cl2,发生反应的离子方程式为:
a Fe2++b Br-+c Cl2 =" d" Fe3++ e Br2+ f Cl-
下列选项中的数字与离子方程式中的a、b、c、d、e、f一一对应,其中不符合反应实际的是( )
| A.2 4 3 2 2 6 | B.0 2 1 0 1 2 |
| C.2 0 1 2 0 2 | D.2 2 2 2 1 4 |
将0.195g锌粉加入到20.0mL的0.100 mol·L-1MO2+溶液中,恰好完全反应,则还原产物可能是( )
| A.M | B.M2+ | C.M3+ | D.MO2+ |
R、X、Y、Z是四种元素,其常见化合价均为+2,且X2+与单质R不反应;X2++Z=X+Z2+,Y+Z2+=Y2++Z,这四种离子被还原成0价时表现的氧化性大小顺序为( )
| A.R2+﹥X2+﹥Z2+﹥Y2+ | B.X2+﹥R2+﹥Y2+﹥Z2+ |
| C.Y2+﹥Z2+﹥R2+﹥X2+ | D.Z2+﹥X2+﹥R2+﹥Y2+ |
在2009年10月1日,新的饮用矿泉水强制性国家标准《饮用天然矿泉水》正式实施,其中“溴酸盐(BrO3-)”这一潜在致癌物质被做了严格限制。有关专家解释,矿泉水在开采过程中会含有少量溴化物(Br-),在后续的生产过程中经臭氧(O3)处理逐渐转化成溴酸盐。下列有关该转化过程的认识正确的是( )
| A.该过程中溴化物(Br-)得到电子 |
| B.该过程中臭氧(O3)是氧化剂,溴酸盐(BrO3-)是还原剂 |
| C.该过程中溴元素被还原,氧元素被氧化 |
| D.该过程中溴元素发生氧化反应,氧元素发生还原反应 |
下列反应既属于氧化还原反应,又是吸热反应的是( )
| A.铝与稀盐酸的反应 | B.灼热的木炭与CO2反应 |
| C.甲烷在氧气中的燃烧反应 | D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应 |