下列相关离子方程式的书写正确的是( )
A.硫化亚铁溶于适量稀硝酸中: → →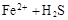 ↑ ↑ |
B.向水中通入少量氯气:Cl2 + H2O 2H+ + Cl﹣+ ClO﹣ 2H+ + Cl﹣+ ClO﹣ |
C.碳酸氢钠溶液中加入过量Ba(OH)2溶液: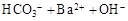 → →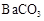 ↓ ↓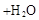 |
D.硫酸溶液中加入过量Ba(OH)2溶液: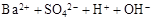 → →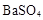 ↓ ↓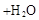 |
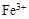 、
、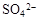 、
、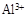 和X四种离子以物质的量之比
和X四种离子以物质的量之比 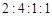 大量共存于同一溶液中,则X
大量共存于同一溶液中,则X
可能是( )
A.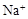 | B.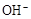 | C.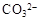 | D.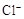 |
下列离子方程式正确的是
| A.在碳酸氢钙溶液中加入少量盐酸:Ca2++2HCO3-+2H+→CO2↑+2H2O+CaCO3↓ |
| B.硫酸铁溶液与氢氧化钡溶液:Fe3++SO42-+Ba2++3OH-→Fe(OH)3↓+BaSO4↓ |
| C.次氯酸钙溶液中通入足量二氧化硫:Ca2++ClO-+SO2+H2O→CaSO4↓+Cl-+2H+ |
| D.氢氧化钠溶液中通入过量二氧化碳:OH-+CO2→HCO3- |
下列离子或物质组能大量共存,且满足相应条件的是
| 选项 | 离子或物质 | 条件 |
| A | Na+、K+、Cl-、SO42- | c(Na+)+c(K+)=c(SO42-)+ c(Cl-) |
| B | Fe3+、SO32-、Cl- | 加入NaOH溶液,产生红褐色沉淀 |
| C | Ba+、HCO3-、Cl-、H+ | 加入氨水产生沉淀 |
| D | SO2、O2、NO2 | 通入足量NaOH溶液后,可能会没有任何气体剩余 |
能正确表示下列各组溶液混合后,所得液体恰好呈中性的离子方程式是
| A.Ba(OH)2和NaHSO4:Ba2+ +2OH— +2H+ +SO42—→BaSO4↓+ 2H2O |
| B.Ba(OH)2和NaHSO4:Ba2+ + OH—+ H++ SO42—→BaSO4↓+ H2O |
| C.Ba(OH)2和KAl(SO4)2:2Ba2++ 4OH—+ Al3++ 2SO42—→2BaSO4↓+ AlO2— |
| D.Ba(OH)2和KAl(SO4)2:3Ba2+ + 6OH—+ 2Al3++ 3SO42—→3BaSO4↓+2Al(OH)3↓ |
今有一混合物的水溶液,只可能含有以下离子中的若干种:NH4+ 、Cl-、Mg2+、Ba2+、K+、CO32-、SO42-,现取三份100 mL溶液进行如下实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加足量NaOH溶液加热后,收集到气体0.04mol
③第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g。
根据上述实验,以下推测正确的是
| A.K+可能存在 | B.该溶液中含CO32-离子的浓度为0.2mol/L |
| C.Cl-一定不存在 | D.Ba2+一定不存在,Mg2+可能存在 |
在由水电离产生的H+的浓度为1×10-13 mol/L的溶液中,一定能大量共存的离子组是
①K+、Cl-、NO3-、S2-;②K+、Fe2+、I-、SO42-;③Na+、Cl-、NO3-、SO42-;④Na+、Ca2+、Cl-、HCO3-;⑤K+、Ba2+、Cl-、NO3-
| A.①③ | B.③⑤ | C.③④ | D.②⑤ |
已知同温度下溶解度:Zn(OH)2>ZnS,MgCO3>Mg(OH)2;就溶解或电离出S2-的能力而言,FeS>H2S>CuS,则下列离子方程式错误的是
| A.Mg2++2HCO3-+2Ca2++4OH- = Mg(OH)2↓+2CaCO3↓+2H2O |
| B.Cu2++H2S = CuS↓+2H+ |
| C.Zn2++S2-+2H2O = Zn(OH)2↓+H2S↑ |
| D.FeS+2H+ = Fe2++H2 S↑ |
