把Ba(OH)2溶液滴入明矾[KAl(SO4)2·12H2O]溶液中,使SO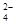 全部转化成BaSO4沉淀,此时铝元素的存在形式是
全部转化成BaSO4沉淀,此时铝元素的存在形式是
A.Al | B.Al(OH)3 | C.AlO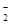 | D.Al 和Al(OH)3 和Al(OH)3 |
下列各组离子在溶液中能大量共存的是
A.Na+、Al3+、Cl-、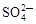 | B.Cu2+、Cl-、 、OH- 、OH- |
C.Ca2+、Na+、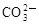 、 、 | D.H+、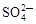 、 、 、OH- 、OH- |
下列反应的离子方程式中,书写正确的是
A.氯气溶于水: |
B.将铝粉投入氢氧化钠溶液中: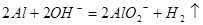 |
C.铜与氯化铁溶液反应: |
D.过氧化钠与水反应: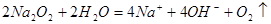 |
下列各组离子在指定的环境中能大量存在的是 ( )
| A.pH=1的无色溶液中:SO42-、Cu2+、Na+、Cl- |
| B.能使酚酞试液变红色的溶液中:Na+、K+、S2-、CO32- |
| C.加入铝粉能产生H2的溶液中:NH4+、Na+、Fe2+、NO3- |
| D.水电离出的c(H+)=1×10-12mol/L的溶液中:K+、Na+、Cl-、HCO3- |
在水溶液中能够大量共存的离子组是
| A.NH4+、Na+、CO32—、Cl— | B.K+、Fe3+、OH—、SO42— |
| C.Na+、Al3+、HCO3—、NO3— | D.H+、Cu2+、S2—、SO42— |
下列叙述正确的是( )
| A.吸热反应一定是反应物总能量大于生成物的总能量 |
| B.明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 |
| C.强电解质溶液导电能力一定很强,弱电解质溶液导电能力一定很弱 |
| D.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 |
下列离子方程式的书写正确的是( )
| A.实验室用大理石和稀盐酸制取CO2:2H+ + CO32-= CO2 + H2O |
| B.铁和稀硫酸反应:Fe + 2H+= H2 + Fe3+ |
| C.NH4HCO3溶液中加入过量的NaOH溶液:NH4+ + OH-= NH3+H2O |
| D.NaHCO3溶液与NaOH溶液反应:OH- + HCO3-= CO32- + H2O |
某溶液仅含Fe2+、Na+、Al3+、Ba2+、SO42-、NO3-、Cl-中的4种离子,所含离子的物质的量均为1mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。下列说法不正确的是
| A.若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色 |
| B.若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色 |
| C.该溶液中所含的离子是:Fe2+、Na+、SO42-、NO3- |
| D.若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为72g |
在离子浓度都为0.1 mol/L的下列溶液中,加入(或通入)某物质后,发生反应先后顺序正确的是
| A.在含Fe3+、Cu2+、H+的溶液中加入锌粉:Cu2+、Fe3+、H+ |
| B.在含I-、SO32-、Br-的溶液中不断通入氯气:I-、Br-、SO32- |
| C.在含AlO2-、SO32-、OH-的溶液中逐滴加入硫酸氢钠溶液:OH-、AlO2-、SO32- |
| D.在含Fe3+、H+、NH4+的溶液中逐渐加入烧碱溶液:H+、NH4+、Fe3+ |
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列条件下关于离子存在的说法中正确的是 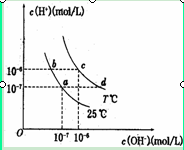
| A.a点对应的溶液中大量存在:Na+、Ba2+、Fe3+、Cl- |
B.b点对应的溶液中大量存在: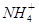 、K+、I-、 、K+、I-、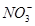 |
| C.c点对应的溶液中大量存在: Cu2+、Na+、Cl-、S2- |
| D.d点对应的溶液中大量存在:K+、AlO2-、ClO-、Cl- |