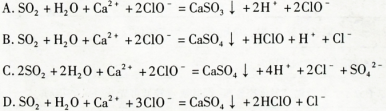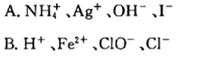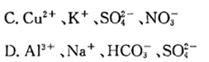下列对各组离子或物质是否能够大量共存解释正确的是( )
| A | 常温常压下NH3、O2、H2、CO2 | 不能共存 | NH3为碱性气体、CO2为酸性气体,二者反应生成(NH4)2CO3 |
| B | c(OH-)=1.0×10-13 mol/L溶液中,Fe2+、NO3—、SO42—、Na+ | 不能共存 | 发生反应:3Fe2++NO3—+4H+=3Fe3++NO↑+2H2O |
| C | 溶液中:K+、Cu2+、Cl-、NH3·H2O | 不能共存 | 发生反应:Cu2++2OH-=Cu(OH)2↓ |
| D | 溶液中:Al3+、Na+、SO42—、HCO3— | 可以共存 | 不能发生反应 |
某溶液可能含有下列离子中的几种(不考虑溶液中微量的H+和OH-):Na+、NH4+、SO42—、CO32—、NO3—。取200 mL该溶液,等体积分成两份,分别做下列实验。
实验一:第一份加入足量烧碱并加热,产生的气体在标准状况下为224 mL。
实验二:第二份先加入足量的盐酸,无现象,再加入足量BaCl2溶液,得沉淀2.33 g。
下列说法正确的是( )
| A.该溶液可能含有Na+ |
| B.该溶液一定含有NH4+、SO42—、CO32—、NO3— |
| C.该溶液一定不含有NO3— |
| D.该溶液一定含有Na+,且c(Na+)≥0.1 mol·L-1 |
下列离子方程式不正确的是( )
| A.FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+=4Fe3++2H2O |
| B.为缓解胃酸过多,服含NaHCO3的抗酸药:HCO3—+H+=H2O+CO2↑ |
| C.过量Na投入AlCl3溶液:Al3++4Na+2H2O=AlO2—+4Na++2H2↑ |
| D.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42—完全沉淀:2Ba2++Al3++2SO42—+4OH-=AlO2—+2BaSO4↓+2H2O |
根据表中信息,判断下列叙述中正确的是( )
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | / | Fe3+、Br2 | |
| ② | KClO3 | 浓盐酸 | / | Cl2 | |
| ③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
A.由表中①组的信息可知通入Cl2的量不同,氧化产物可能不同
B.氧化性强弱的比较:KClO3>Fe3+>Cl2>Br2
C.表中②组反应的还原产物是KCl,电子转移数目是6e-
D.表中③组反应的离子方程式为2MnO4—+3H2O2+6H+=2Mn2++4O2↑+6H2O
下列分子或离子在指定的分散系中能大量共存的一组是
( )
| A.银氨溶液:Na+、K+、NO3—、NH3·H2O |
| B.空气:C2H2、CO2、SO2、NO |
| C.氢氧化铁胶体:H+、K+、S2-、Br- |
| D.高锰酸钾溶液:H+、Na+、SO42—、葡萄糖分子 |
能正确表示下列反应的离子方程式是( )
| A.用过量氨水吸收工业尾气中的SO2:2NH3·H2O+SO2=2NH4++SO32—+H2O |
| B.氯化钠与浓硫酸混合加热:H2SO4+2Cl-△,SO2↑+Cl2↑+H2O |
| C.磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3—=3Fe3++NO↑+3H2O |
| D.明矾溶液中滴入Ba(OH)2溶液使SO42—恰好完全沉淀:2Ba2++3OH-+Al3++2SO42—=2BaSO4↓+Al(OH)3↓ |
下列有关叙述正确的是( )
| A.氯化钠的水溶液能导电,食盐水是电解质 |
| B.氯气的水溶液能导电,但氯气是非电解质 |
| C.H2SO4液态时不导电,它是非电解质 |
| D.MgCl2在熔融状态下可导电,它是电解质 |
微粒甲与离子乙在溶液中的转化关系如图所示: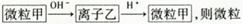 甲是
甲是
| A.Si | B.NH4+ | C.Al | D.SO2 |