下列离子方程式正确的是( )
| A.向碳酸氢钙溶液中加入少量氢氧化钠溶液:Ca2++2HCO3—+2OH-=CaCO3↓+CO32—+2H2O |
| B.向偏铝酸钠溶液中通入过量二氧化碳气体:AlO2—+CO2+2H2O=Al(OH)3↓+HCO3— |
C.以石墨作电极电解氯化铝溶液:2Cl-+2H2O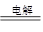 2OH-+H2↑+Cl2↑ 2OH-+H2↑+Cl2↑ |
| D.漂白粉溶液中通入足量二氧化硫气体:ClO-+SO2+H2O=HClO+HSO3— |
下列事实相对应的离子方程式,不正确的是( )
A.将NaHSO3溶于水,溶液呈弱酸性:HSO3—+H2O SO32—+H3O+ SO32—+H3O+ |
| B.工业上用热的纯碱溶液吸收溴蒸气生成溴酸钠:3Br2+3CO32—=5Br-+BrO3—+3CO2 |
| C.明矾溶液中加Ba(OH)2溶液至SO42—完全沉淀:Al3++2SO42—+2Ba2++3OH-=2BaSO4↓+Al(OH)3↓ |
D.用惰性电极电解MgCl2溶液产生气体和白色沉淀:Mg2++2Cl-+2H2O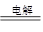 Cl2↑+H2↑+Mg(OH)2↓ Cl2↑+H2↑+Mg(OH)2↓ |
已知电离平衡常数:H2CO3>HClO>HCO3—,氧化性:HClO>Cl2>Br2>Fe3+>I2。下列有关离子反应或离子方程式的叙述中,正确的是( )
| A.向FeI2溶液中滴加少量氯水,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl- |
| B.向溴水中加入足量氯化亚铁溶液能使溴水变成无色 |
| C.向NaClO溶液中通入少量CO2的离子方程式:2ClO-+CO2+H2O=2HClO+CO32— |
| D.能使pH试纸显深红色的溶液中,Fe3+、Cl-、Ba2+、Br-能大量共存 |
下列各组离子在指定条件下能大量共存的是( )
①漂白粉的水溶液中:Fe2+、Cl-、Ca2+、Na+
②滴加石蕊试液呈红色的溶液:K+、N 、Cl-、S2-
、Cl-、S2-
③常温下能够与金属Mg反应放出气体的溶液:Fe3+、Al3+、S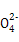 、K+
、K+
④常温下pH=2的溶液中:N 、Na+、Cl-、Cu2+
、Na+、Cl-、Cu2+
⑤无色溶液中:K+、CH3COO-、HC 、Mn
、Mn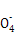
| A.②③ | B.①③ | C.③④ | D.①⑤ |
下列实验现象所对应的离子方程式不正确的是( )
| | 实验 | 现象 | 离子方程式 |
| A |  H2SO4 KI淀粉溶液 | 在空气中放置一段时间后溶液呈蓝色 | 4H++4I-+O2 2I2+2H2O 2I2+2H2O |
| B |  稀盐酸 稀碳酸钠溶液 | 开始时无气泡,后来有气泡 | C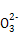 +H+ +H+ HC HC HC  +H+ +H+ CO2↑+H2O CO2↑+H2O |
| C | 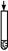 NaOH溶液 氯水 | 溶液由淡黄绿色变为无色 | Cl2+2OH- Cl-+ClO-+H2O Cl-+ClO-+H2O |
| D |  H2SO4加有 酚酞的Ba(OH)2 溶液 | 有白色沉淀生成,溶液由红色变为无色 | Ba2++OH-+H++S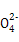  BaSO4↓+H2O BaSO4↓+H2O |
常温时,下列各组离子在指定溶液中一定能大量共存的是( )
A.pH=0的溶液中:Na+、Fe2+、N 、ClO- 、ClO- |
B.c(Fe3+)="0.1" mol/L的溶液中:K+、Ba2+、S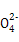 、SCN- 、SCN- |
C.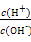 =1012的溶液中:N =1012的溶液中:N 、Al3+、S 、Al3+、S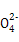 、Cl- 、Cl- |
D.由水电离的c(H+)=1×10-14 mol/L的溶液中:Ca2+、K+、Cl-、HS |
下列离子方程式书写正确的是( )
A.Na2O2与H2O反应:2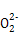 +2H2O +2H2O 4OH-+O2↑ 4OH-+O2↑ |
B.FeCl2溶液与稀硝酸反应:Fe2++N +4H+ +4H+ Fe3++NO↑+2H2O Fe3++NO↑+2H2O |
C.CaCO3与醋酸溶液反应:CaCO3+2H+ Ca2++CO2↑+H2O Ca2++CO2↑+H2O |
D.KAl(SO4)2溶液与氨水反应:Al3++3NH3·H2O Al(OH)3↓+3N Al(OH)3↓+3N |
室温时,下列各组离子在指定溶液中可以大量共存的是( )
A.由水电离出的c(H+)=10-12 mol/L的溶液中:Na+、Ba2+、HC 、C1- 、C1- |
B.无色透明溶液中:K+、Cu2+、S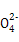 、Na+ 、Na+ |
C.含有大量Al 的溶液中:Na+、OH-、Cl-、C 的溶液中:Na+、OH-、Cl-、C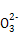 |
D.能使pH试纸显红色的溶液中:Na+、ClO-、Fe2+、S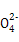 |
下列离子方程式均正确的是( )
A.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+ Cu2++2Fe2+ Cu2++2Fe2+ |
B.铜与浓硝酸反应:Cu+N +2H+ +2H+ Cu2++NO2↑+H2O Cu2++NO2↑+H2O |
C.向NaAlO2溶液中通入过量CO2:2Al +CO2+3H2O +CO2+3H2O 2Al(OH)3↓+C 2Al(OH)3↓+C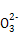 |
D.NaHCO3的水解:HC +H2O +H2O H3O++C H3O++C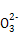 |
能正确表示下列反应的离子方程式的为( )
A.硫化亚铁溶于稀硝酸中:FeS+2H+ Fe2++H2S↑ Fe2++H2S↑ |
B.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O Al Al +4N +4N +2H2O +2H2O |
C.硫代硫酸钠溶液中滴入稀盐酸:S2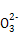 +2H+ +2H+ S↓+SO2↑+H2O S↓+SO2↑+H2O |
D.在NaHSO4溶液中滴加Ba(OH)2至中性:H++S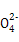 +Ba2++OH- +Ba2++OH- BaSO4↓+H2O BaSO4↓+H2O |