下列各组中的离子,能在溶液中大量共存的是( )
| A.H+Na+CO32-Cl- | B.Ba2+Na+Cl-SO42- |
| C.K+ H+ SO42-OH- | D.Ag+ Al3+ NO3-H+ |
体积相同的甲、乙两份植物营养液,其所含组分的物质的量浓度如下表:
| | KCl | K2SO4 | ZnCl2 | ZnSO4 |
| 甲 | 0.3 mol·L-1 | 0.2 mol·L-1 | 0 | 0.1 mol·L-1 |
| 乙 | 0.1 mol·L-1 | 0.3 mol·L-1 | 0.1 mol·L-1 | 0 |
下列对两份营养液成分的分析中,正确的是
A.两种溶液的n(Zn2+)不同
B.两种溶液的c(Cl-)之比为3:1
C.甲溶液的c(K+)="0.5" mol·L-1
D.两种溶液所含的N(SO42-)相等
能正确表示下列化学反应的离子方程式是
| A.饱和石灰水跟稀硝酸反应Ca(OH)2 + 2H+ = Ca2+ + 2H2O |
| B.钠和水反应Na+2H2O=Na++H2↑+2OH- |
| C.大理石与盐酸反应 CaCO3+2H+=Ca2++H2O+CO2↑ |
| D.硫酸与氢氧化钡溶液反应 Ba2++OH-+H++SO42-= BaSO4↓+ H2O |
下列反应的离子方程式正确的是
| A.向酸化的FeSO4中加入H2O2溶液:2Fe2++2H++H2O2 =2Fe3++2H2O |
| B.向NaHCO3溶液中加入足量Ba(OH)2的溶液:Ba2++2HCO3-+2OH-=2H2O+BaCO3↓+ CO32- |
| C.向苯酚钠溶液中通入少量的CO2:2C6H5O-+CO2+H2O—→2C6H5OH+CO32- |
| D.向NaOH溶液中滴加少量氯化铝溶液:Al(OH)3+3OH-=Al(OH)3↓ |
下列情况下,离子组间一定能在溶液中同时大量共存的是
| A.pH=2的溶液中:SO42-、K+、NO3-、Mg2+ |
| B.pH试纸呈现红色的溶液:Fe2+、K+、NO3-、Na+ |
| C.水电离出的c(H+)=10-14mol/L的溶液中:Na+、HCO3-、Cl-、SO42- |
| D.CO32-可以大量存在的溶液:Ag+、K+、NO3-、Al3+ |
下列事实、离子方程式及其对应关系均正确的是:
| A.铁溶于稀硝酸,溶液变为浅绿色:Fe + 4H+ + NO3—= Fe3+ + NO ↑ + 2H2O |
B.向K2Cr2O7溶液中滴加少量浓H2SO4,溶液变为黄色: Cr2O72-(橙色) + H2O  2CrO42-(黄色) +2H+ 2CrO42-(黄色) +2H+ |
| C.向淀粉碘化钾溶液中滴加稀硫酸,在空气中放置一段时间后溶液变蓝:4H+ + 4I- + O2 =2I2 + 2H2O |
D.向水杨酸(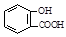 )中滴加NaHCO3溶液,放出无色气体: )中滴加NaHCO3溶液,放出无色气体: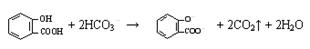 |
 是一种食品添加剂,它与酸性
是一种食品添加剂,它与酸性 溶液的反应方程式为:
溶液的反应方程式为: ,下列叙述中正确的是
,下列叙述中正确的是
A.生成l mo1 需消耗0.4mo1 需消耗0.4mo1 |
| B.反应过程中溶液的pH减小 |
C.该反应中NO 被还原 被还原 |
D.X表示的粒子是 |
下列各组粒子在指定溶液中能大量共存的是
A.pH=l的溶液中: |
B.加入A1能放出H2的溶液中: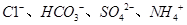 |
C.含有大量 的溶液中: 的溶液中: |
D.由水电离出的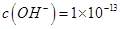 mol mol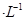 的溶液中: 的溶液中: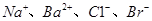 |
下列解释实验事实的方程式不正确的是
A.明矾的水溶液 |
B.将NH3通入滴有酚酞的水中,溶液变红: |
C.向 溶液中加入NaC1溶液后,再加Na2S溶液,白色沉淀转化为黑色沉淀: 溶液中加入NaC1溶液后,再加Na2S溶液,白色沉淀转化为黑色沉淀: = = |
D.用醋酸检验牙膏中的摩擦剂碳酸钙: = = |
下列离子方程式的书写及评价,均合理的是
| 选项 | 离子方程式 | 评价 |
| A | 将2molCl2通入到含1molFeI2的溶液中: 2Fe2++2I—+2Cl2 = 2Fe3++4Cl-+I2 | 正确;Cl2过量,可将Fe2+ 、I—均氧化 |
| B | Mg(HCO3)2溶液与足量的NaOH溶液反应: Mg2++ HCO3—+ OH—= MgCO3↓+ H2O | 正确;酸式盐与碱反应生成正盐和水 |
| C | 过量SO2通入到NaClO溶液中: SO2 + H2O + ClO- = HClO+HSO3- | 正确; 说明酸性: H2SO3强于HClO |
| D | 1mol/L的NaAlO2溶液和2.5mol/L的HCl溶液等体积互相均匀混合:2AlO2- + 5H+ = Al3+ + Al(OH)3↓+ H2O | 正确;AlO2-与Al(OH)3消耗的H+的物质的量之比为2:3 |