向含有等物质的量的NH4+、Al3+、H+的混合溶液中,慢慢滴加NaOH溶液直至过量,
并不断搅拌,依次发生了数个离子反应,则第三个离子反应是( )
| A.H++OH-=H2O |
| B.Al3++3OH-=Al(OH)3↓ |
| C.Al(OH)3+OH-=AlO2-+2H2O |
| D.NH4++OH-=NH3·H2O |
下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是( )
| | A | B | C | D |
| 强电解质 | Fe | NaCl | CaCO3 | HNO3 |
| 弱电解质 | CH3COOH | NH3 | H3PO4 | Fe(OH)3 |
| 非电解质 | C12H22O11 (蔗糖) | BaSO4 | C2H5OH | H2O |
甲、乙、丙、丁四种易溶于水的物质,分别由NH4+、Ba2+、Mg2+、H+、OH-、Cl-,HCO3-、SO42-中的不同阳离子和阴离子各一种组成,已知;①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;②0.1 mol/L乙溶液中c(H+)>0.1 mol/L;③向丙容器中滴入AgNO3溶液有不溶于稀硝酸的白色沉淀生成,下列结论不正确的是( )
| A.甲溶液含有Ba2+ | B.乙溶液含有SO42- |
| C.丙溶液含有Cl- | D.丁溶液含有Mg2+ |
将足量CO2通入下列溶液中,所含离子还能大量共存的是( )
| A.K+、SiO32-、Cl-、NO3- |
| B.H+、NH4+、Al3+、SO42- |
| C.Na+、S2-、OH-、SO42- |
| D.Na+、CO32-、CH3COO-、HCO3- |
下列对实验现象的预测不正确的是( )
| A.向Na2SiO3溶液中通入CO2,溶液变浑浊,继续通入CO2至过量,浑浊消失 |
| B.向Na2CO3饱和溶液中通入CO2,溶液变浑浊,继续通入CO2,有晶体析出 |
| C.向Ca(ClO)2溶液中通入CO2,溶液变浑浊,再加入品红溶液,红色褪去 |
| D.向Ca(OH)2溶液中通入CO2,溶液变浑浊,继续通入CO2至过量,浑浊消失,再加入过量NaOH溶液,溶液又变浑浊 |
向存在大量K+、Cl-的溶液中通入足量CO2后,该溶液中还可能大量存在的离子组是( )
| A.Na+、Br-、CO32- | B.AlO2-、Na+、MnO4- |
| C.NH4+、Na+、SO42- | D.Na+、Ag+、NO3- |
在200 mL 含Mg2+、Al3+、NH4+、H+、Cl-的溶液中,逐滴加入5 mol·L-1 NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示。下列叙述不正确的是( )
| A.x-y=0.01 mol |
| B.原溶液中c(Cl-)=0.75 mol·L-1 |
| C.原溶液的pH=1 |
| D.原溶液中n(Mg2+)∶n(Al3+)=5∶1 |
下列图示与对应的叙述相符的是( )
| A.图Ⅰ表示常温下盐酸滴加到0.1 mol·L-1某碱溶液中得到的滴定曲线,由图Ⅰ可知二者恰好中和时,所得溶液的pH>7 |
B.图Ⅱ表示一定条件下进行的反应2SO2+O2 2SO3 ΔH<0各成分的物质的量变化,t2时刻改变的条件可能是升高温度 2SO3 ΔH<0各成分的物质的量变化,t2时刻改变的条件可能是升高温度 |
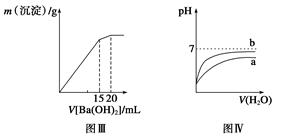
| C.图Ⅲ表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20 mL Ba(OH)2溶液时,沉淀全部是BaSO4 |
| D.图Ⅳ表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是盐酸 |
下列图示与对应叙述相符的是( )

| A.图1反应达到平衡后,升高温度,平衡常数K值变大 |
| B.图2表示镁条放入盐酸中生成氢气速率随时间的变化 |
| C.图3表示向Ca(HCO3)2溶液中滴入NaOH溶液所得沉淀的质量的变化 |
| D.图4表示纯碱溶液受热时氢氧根浓度随温度的变化 |
