在水溶液中能大量共存的一组离子是
| A.S2—、Al3+、ClO-、Cl- | B.K+、Mg2+、OH-、NO3- |
| C.H+、Mg2+、SiO32-、SO42- | D.NH4+、Na+、Cl-、SO42- |
下列各组离子,在碱性条件下能大量共存,在强酸性条件下发生氧化还原反应的是
| A.Mg2+、Na+、SO42-、HCO3— | B.Na+、K+、NO3—、SO32— |
| C.K+、Na+、SiO32—、ClO— | D.NH4+、Na+、SO42—、NO3— |
水溶液中能大量共存的一组离子是
| A.H+、NO3-、I-、Cl- |
| B.Cu2+、Br-、H+、SO42- |
| C.Al3+、Mg2+、CO32-、NO3- |
| D.NH4+、Cl-、OH-、HCO3- |
下列微粒在水溶液中能大量共存的是
| A.Fe3+、H+、I-、Na+ |
| B.Al3+、Na+、AlO2-、SO42- |
| C.K+、NH4+、H+、CO32— |
| D.Cu2+、SO42—、Al3+、Cl— |
常温下,下列各组离子在指定溶液中能大量共存的是
| A.pH=1的溶液中:Fe2+、NO3-、SO42-、Na+ |
| B.水电离出的c(H+)=10-12mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| C.c(H+)/c(OH-)=1012的水溶液中:NH4+、Al3+、NO3-、Cl- |
| D.c(Fe3+)=0.1mol/L的溶液中:K+、ClO-、SO42-、SCN- |
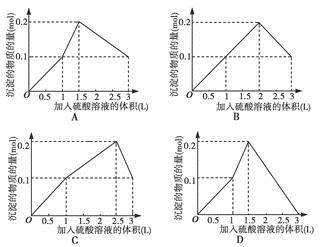
下列图示与对应的叙述相符的是
| A.图I表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| B.图Ⅱ表示表示向KAl(SO4)2溶液中滴加Ba(OH)2溶液产生沉淀的物质的量(n)随氢Ba(OH)2溶液体积(V)的变化 |
| C.图Ⅲ表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液 |
| D.图Ⅳ表示某可逆反应生成物的物质的量随反应时间变化的曲线,t时刻反应正速率最大 |
将足量CO2通入NaOH和Ba(OH)2的混合稀溶液中,生成沉淀的物质的量(n)和通入CO2气体的体积(V)的关系如下图所示,图中AB段表示的离子方程式先后顺序正确的是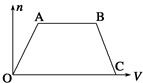
①CO2+OH-=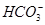 ②CO2+2OH-=
②CO2+2OH-=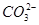 +H2O
+H2O
③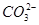 +Ba2+=BaCO3↓ ④BaCO3+CO2+H2O=Ba2++2
+Ba2+=BaCO3↓ ④BaCO3+CO2+H2O=Ba2++2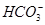
⑤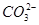 +CO2+H2O=2
+CO2+H2O=2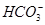
| A.③① | B.②⑤ | C.⑤④ | D.④② |
下列反应的离子方程式正确的是
| A.稀硫酸与铁反应:2Fe+6H+=2Fe3++3H2↑ |
| B.2 mol·L-1的AlCl3溶液和7 mol·L-1的NaOH溶液等体积均匀混合: 2Al3++7OH-=Al(OH)3↓+  +2H2O +2H2O |
| C.Ba(OH)2溶液中加入少量的NaHSO4溶液: Ba2++2OH-+2H++  =BaSO4↓+2H2O =BaSO4↓+2H2O |
D.NaHCO3的水解: +H2O +H2O   +H3O+ +H3O+ |
向含Na2CO3、NaAlO2的混合溶液中逐滴加入150 mL 1 mol·L-1HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法中不正确的是
A.a曲线表示的离子方程式为: +H++H2O +H++H2O Al(OH)3↓ Al(OH)3↓ |
| B.b和c曲线表示的离子反应是相同的 |
| C.M点时,溶液中沉淀的质量为3.9 g |
D.原混合溶液中的 与 与 的物质的量之比为1∶2 的物质的量之比为1∶2 |