下列表示对应化学反应的离子方程式正确的是
| A.向铁粉中加入足量稀硝酸:2Fe+6H+=2Fe3++3H2↑ |
| B.向AlCl3溶液中滴加浓氨水至过量:Al3++4OH-=AlO2-+2H2O |
| C.向NaIO3溶液中加入适量NaHSO3溶液:IO3-+3HSO3-=I-+3SO42-+3H+ |
| D.向NH4HCO3溶液中滴加过量NaOH溶液:NH4++HCO3-+2OH-=CO32-+NH3·H2O |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.澄清透明的溶液中:H+、Fe2+、SO42-、NO3- |
| B.使甲基橙变红的溶液中:Ca2+、NH4+、CH3COO-、Cl- |
| C.0.1 mol·L-1的BaCl2溶液中:K+、Na+、OH-、NO3ˉ |
| D.由水电离出的c(H+)=10-12 mol·L-1的溶液中:Mg2+、K+、Br-、HCO3- |
下列离子方程式正确的是( )
| A.过氧化钠和水反应:2Na2O2+2H2O=4Na++4 OH—+O2↑ |
| B.用铜为电极电解饱和食盐水:2Cl—+2H2O通电Cl2↑+H2↑+2OH— |
| C.在明矾溶液中滴加过量氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+ |
| D.向小苏打溶液中加少量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.在pH=1的溶液中:K+、Na+、SO42–、HCO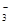 |
B.在0.1 mol·L-1 Na2CO3溶液中:Al3+、K+、NO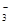 、SO42– 、SO42– |
C.在0.1 mol·L-1 FeCl3溶液中:K+、NH 、I-、SCN- 、I-、SCN- |
D.在c( H+)/c(OH-)=10-12的溶液中:K+、Na+、ClO-、NO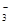 |
下列说法正确的是( )
| A.二氧化硫具有较强的还原性,故不能用浓硫酸干燥 |
| B.含极性键的共价化合物一定是电解质 |
| C.氯化钠、冰醋酸、酒精分别属于强电解质、弱电解质、非电解质 |
| D.天然气、酒精和液化石油气分别属于化石能源、不可再生能源和二次能源 |
常温时,下列各组离子能大量共存的是
A.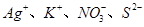 | B.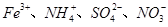 |
C.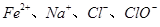 | D. |
在碱性溶液中能大量共存且为无色透明的溶液是
| A.K+、Cl-、MnO4-、SO42- | B.Na+、SiO32-、NO3-、CO32- |
| C.Na+、NO3-、SO42-、HCO3- | D.Na+、SO42-、S2-、ClO- |
下列离子方程式正确的是
| A.为缓解胃酸过多,服含NaHCO3的抗酸药:HCO3-+H+=H2O+CO2↑ |
| B.FeSO4溶液被氧气氧化:4Fe2++O2+2H2O=4Fe3++4OH- |
| C.硫酸铝溶液中加入过量的氨水:Al3++3OH-=Al(OH)3↓ |
| D.将Na2O2加入H2O中:Na2O2+H2O=2Na++2OH-+O2↑ |
某溶液中含有的离子可能是K+、Ba2+、A13+、Mg2+、AlO2-、CO32-、SiO32-、Cl-中的几种,现进行如下实验:
①取少量溶液加氢氧化钠溶液过程中无沉淀生成
②另取少量原溶液,逐滴加入5mL 0.2mol·L-1盐酸,发生的现象是:开始产生沉淀并逐渐增多,沉淀量基本不变后产生气体,最后沉淀逐渐减少至消失。
③在上述②沉淀消失后的溶液中,再加入足量的硝酸银溶液可得到沉淀0.43g。
下列说法中正确的是
| A.该溶液中一定不含Ba2+、Mg2+、A13+、SiO32-、Cl- |
| B.该溶液中一定含有K+、AlO2-、CO32-、Cl- |
| C.该溶液是否有K+需做焰色反应(透过蓝色钴玻璃片) |
| D.可能含有Cl- |
某溶液,只可能含有以下离子中的若干种:H+、NH4+、K+、Mg2+、NO2-、CO32-、NO3-,现取两份100mL溶液进行如下实验:①第一份加足量AgNO3溶液后,有5.84g白色沉淀产生,沉淀中加入足量稀盐酸充分反应,有棕色气体产生,沉淀颜色不变,但是质量减少0.1g; ②将产生的气体全部通入过量的澄清石灰水,又得到白色沉淀1.0g,该沉淀能溶于稀盐酸产生无色气体;③第二份加入过量浓NaOH溶液,加热使产生的气体全部放出,用50mL0.5mol·L-1的硫酸溶液恰好完全吸收,酸也不剩余。根据上述实验,以下推测不正确的是( )
| A.原溶液一定不存在较大浓度的H+、Mg2+ |
| B.原溶液确定含NH4+、NO2-、CO32-,且物质的量之比为5︰2︰1 |
| C.不能确定原溶液是否含有K+、NO3- |
| D.实验中产生的棕色气体遇空气颜色会加深 |