用NA表示阿伏加德罗常数,下列说法正确的是
| A.500mL2mol/L葡萄糖溶液中所含分子数为NA |
| B.0.1mol/L Na2CO3溶液中的阴离子总数大于0.1NA |
| C.电解精炼铜时,若阳极质量减少64g,则外电路导线上不一定通过2NA个电子 |
| D.5.6g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A.1mol Cl2通入水中,充分反应后转移电子数为NA |
| B.常温下,1.12L NO2气体含分子数为0.05NA |
| C.1L 0.5mol·L-1碳酸氢钠溶液中含离子数为NA |
| D.通常状况下16gO2和O3混合气体中含氧原子数为NA |
下列化学用语表示正确的是 ( )
| A.HClO的结构式:H—O—Cl |
B.四氯化碳的电子式: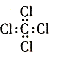 |
C.CO2的比例模型: |
| D.乙烯的结构简式:CH2CH2 |
下列电子式书写正确的是
A.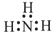 | B. | C.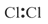 | D. |
设NA为阿伏加德罗常数的值,下列有关叙述正确的是
| A.1mol Cl2溶于足量水中转移电子数为NA |
| B.在熔融状态下,1molKHSO4完全电离出的阳离子数为2NA |
| C.标准状况下,22.4LNO与CO2的混合气体中含有的原子数为2NA |
| D.CaC2含有的π键的数目为0.2NA |
若NA为阿伏加德罗常数的值,下列叙述正确的是
| A.1 mol-OH中含有的质子数为9NA |
| B.lmol2,3—丁二醇分子中含C一C数目为4NA |
| C.1 L 1 mol.L-1FeCl3溶液中含有 Fe3 +数为NA |
| D.71 g氯气参与反应,电子转移数目一定为2NA |
下列说法不正确的是(设NA为阿伏加德罗常数的数值)( )
| A.20g重水含有10NA个电子 |
| B.1L 0.1 mol·L-1 Na2SO3溶液中含有的SO32-数目少于0.1NA个 |
| C.使用容量瓶配制溶液时,俯视刻度线定容后所得溶液浓度偏高 |
| D.用足量铜粉除去FeCl2溶液中的FeCl3杂质 |
设NA为阿伏伽德罗常数的数值,下列说法中,正确的是
| A.标准状况下,22.4L Cl2完全溶于水时,转移的电子数为NA |
| B.常温下,1L pH=1的H2SO4溶液中含有H+的数目为0.2NA |
| C.标准状况下,2.24LNH3中含有的共价键数目为NA |
| D.常温下,23gNO2和N2O4的混合气体中含有NA个氧原子 |
设NA为阿伏伽德罗常数的值,下列说法中正确的是
| A.常温常压下,11.2L的NO2和CO2混合气体含有NA个O原子 |
| B.标准状况下,22.4L的乙烯中含有的共用电子对数为12NA |
| C.1L0.1mo1·L-1的氨水中含有0.1NA个OH- |
| D.以石墨为电极电解氯化铜溶液时,若阳极上失去电子NA个,则阴极质量增加32g |
一定温度下,硫酸铜受热分解生成CuO、SO2、SO3和O2。已知:SO2、SO3都能被碱石灰和氢氧化钠溶液吸收。利用下图装置加热硫酸铜粉末直至完全分解。硫酸铜粉末质量为10.0g,完全分解后,各装置的质量变化关系如下表所示。
| 装置 | A(试管+粉末) | B | C |
| 反应前 | 42.0g | 75.0g | 140.0g |
| 反应后 | 37.0g | 79.5g | 140.0g |
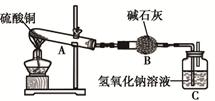
请通过计算,推断出该实验条件下硫酸铜分解的化学方程式是
A.3CuSO4
 3CuO + SO3↑ + 2SO2↑ + O2↑
3CuO + SO3↑ + 2SO2↑ + O2↑B.4CuSO4
 4CuO + 2SO3↑ + 2SO2↑ + O2↑
4CuO + 2SO3↑ + 2SO2↑ + O2↑C.5CuSO4
 5CuO + SO3↑ + 4SO2↑ + 2O2 ↑
5CuO + SO3↑ + 4SO2↑ + 2O2 ↑D.6CuSO4
 6CuO + 4SO3↑ + 2SO2↑ + O2↑
6CuO + 4SO3↑ + 2SO2↑ + O2↑