NA力阿伏加德罗常数,下列叙述正确的是
| A.1mol苯含有的C=C键数为3NA |
| B.1mol Na2O2与水完全反应时转移的电子数为NA |
| C.含NA个Na+的Na2O溶解于1L水中,Na+浓度为1mol·L-1 |
| D.1mol O2和2mol SO2在密闭容器中充分反应后的分子数等于2NA |
下列有关化学用语使用正确的是 ( )
A.HClO的电子式: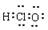 |
B.具有16个质子、16个中子和18个电子的微粒是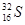 |
C.邻羟基苯甲酸的结构简式: |
D.乙烯的比例模型: |
NA代表阿伏加德罗常数,下列说法正确的是:( )
| A.分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g |
B.已知2CO(g)+O2(g)  2CO2(g);△H=-akJ﹒mol-1将2NA个CO与NA个O2混合充分反应放出akJ的热量。 2CO2(g);△H=-akJ﹒mol-1将2NA个CO与NA个O2混合充分反应放出akJ的热量。 |
| C.用石灰乳完全吸收l mol Cl2时,转移电子的数目是NA |
| D.常温下,0.1mol/LNa2CO3溶液中,含有阴离子的总数大于0.1NA |
下列有关化学用语表示不正确的是
A.氯离子的结构示意图: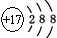 |
B.K2O的电子式: |
C.CO2分子的结构式: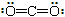 |
D.苯分子的比例模型: |
将7.8g Na2O2和2.7g Al同时放入一定量的水中,充分反应后得到100mL溶液,再向该溶液中缓慢通入HCl气体3.36L(标准状况),若忽略反应过程中溶液的体积变化,则下列判断正确的是
| A.反应过程中得到3.36L(标准状况)的气体 |
| B.反应结束得到3.9g的沉淀 |
| C.反应结束得到的溶液中c(Na+)= c(Cl-)+ c(OH-) |
| D.反应结束得到的溶液中c(NaCl)="1.0" mol·L-1 |
化学用语是学习化学的重要工具,下列表示物质变化的化学用语中,正确的是
A.BaSO4悬浊液中存在平衡:BaSO4(aq)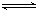 Ba2+(aq)+SO42-(aq) Ba2+(aq)+SO42-(aq) |
B.向K2Cr2O7溶液中加入少量NaOH浓溶液,溶液由橙色变为黄色:Cr2O72-+H2O 2CrO42-+2H+ 2CrO42-+2H+ |
| C.等浓度的NH4Al(SO4)2溶液与Ba(OH)2溶液以1:2体积比混合出现白色沉淀:Al3++2SO42-+2Ba2++3OH-=2BaSO4↓+Al(OH)3↓ |
D.铝热反应的原理为:Al2O3+2Fe 2Al+Fe2O3 2Al+Fe2O3 |
设NA为阿伏加德罗常数的值,下列说法正确的是
| A.lmol氧气与金属钠反应,氧气得到的电子数一定是4NA |
| B.常温下,92gNO2和N2O4混合气体中含有氧原子数为2NA |
| C.在H2O2+Cl2==2HCl+O2反应中,每生成16g氧气,则转移电子数为2NA |
| D.100mL18.4mol·L-1的硫酸与足量铜反应,生成二氧化硫的分子数小于0.92NA |
下列化学用语使用不正确的是
A.Na+的结构示意图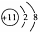 |
| B.纯碱的化学式为Na2CO3 |
C.聚乙烯的结构简式为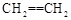 |
D.高氯酸(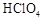 )中氯元素的化合价为+7 )中氯元素的化合价为+7 |
设NA为阿伏加德罗常数的值,下列叙述不正确的是( )
| A.常温常压下,17 g甲基(—14CH3)所含的中子数为8 NA |
| B.室温下,31.0g白磷中含有的共价键数目为1.5NA |
| C.标准状况下,44.8 L NO与22.4 LO2混合后气体中分子总数为2NA |
| D.1 molNa2O和Na2O2混合物中含有的阴、阳离子总数是3NA |
设N0表示阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,0.1 mol Cl2被氢氧化钠溶液完全吸收,转移的电子数目为0.2N0 |
| B.常温常压下,16 g CH4中含有的原子总数为5N0 |
| C.标准状况下,11.2 LCH3OH中含有的氢原子数目为2N0 |
| D.常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1N0 |