题目内容
设N0表示阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,0.1 mol Cl2被氢氧化钠溶液完全吸收,转移的电子数目为0.2N0 |
| B.常温常压下,16 g CH4中含有的原子总数为5N0 |
| C.标准状况下,11.2 LCH3OH中含有的氢原子数目为2N0 |
| D.常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1N0 |
B
解析试题分析:A、Cl2与氢氧化钠溶液发生歧化反应,转移的电子数目为0.1N0,错误;B、气体的质量与条件无关,正确;C、甲醇是液体,错误;D、标准状况下气体摩尔体积是22.4mol/L,常温常压下气体摩尔体积不是22.4mol/L,错误。
考点:考查阿伏加德罗常数有关问题。

练习册系列答案
相关题目
下列说法不正确的是
| A.等质量的乙烯和丙烯中含有的共用电子对数目相等 |
| B.等质量的 14NO和 13CO气体中含有的中子数相等 |
| C.10.6 gNa2CO3固体中含阴阳离子总数约为1.806×1023 |
| D.5.6 g铁和6.4 g铜分别与0.1 mol氯气完全反应,转移的电子数相等 |
下列有关化学用语表示正确的是
| A.丙烯醛的结构简式:CH2CHCHO |
B.含78个中子的碘的核素: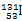 |
| C.氮气分子的电子式::N:::N: |
D.Mg2+的结构示意图: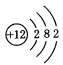 |
将7.8g Na2O2和2.7g Al同时放入一定量的水中,充分反应后得到100mL溶液,再向该溶液中缓慢通入HCl气体3.36L(标准状况),若忽略反应过程中溶液的体积变化,则下列判断正确的是
| A.反应过程中得到3.36L(标准状况)的气体 |
| B.反应结束得到3.9g的沉淀 |
| C.反应结束得到的溶液中c(Na+)= c(Cl-)+ c(OH-) |
| D.反应结束得到的溶液中c(NaCl)="1.0" mol·L-1 |
室温下,抽去下图所示装置中的玻璃片,使两种气体充分反应。下列说法正确的是(设NA表示阿伏加德罗常数的值)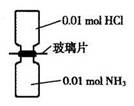
| A.气体反应物的总体积为0.448L |
| B.装置中氢元素的总质量为0.04g |
| C.生成物中含有0.01NA个分子 |
| D.生成物完全溶于永后所得溶液含有0.01 NA个NH4+ |
设NA为阿伏加德罗常数的数值,下列说法中正确的是
| A.电解精炼粗铜时,每转移NA个电子,阳极溶解32g铜 |
| B.1L0.1mo1·L-1的氨水中含OH-离子数为0.lNA个 |
| C.常温常压下,a mo1O2与2a mo1NO混合,降温得到混合气体中氧原子数小于4aNA |
D.在反应5NH4NO3 2HNO3+4N2↑+9H2O中,每生成4molN2,转移电子数为15NA 2HNO3+4N2↑+9H2O中,每生成4molN2,转移电子数为15NA |
设nA为阿伏加德罗常数的数值,下列说法正确的是
| A.常温下,18gH2O中含有2nA个氢原子 |
| B.标准状况下,22.4L苯含有nA个苯分子 |
| C.1mol Na与足量水反应转移2nA个电子 |
| D.0.1 mol?L-1CH3COOH溶液中含有0.1nA个CH3COO- |
下列化学用语正确的是
A.重水的分子式: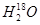 |
B.Mg2+的结构示意图: |
| C.乙酸的分子式:CH3COOH |
D.HCIO的电子式: |
用 NA表示阿伏加德罗常数的值。下列说法正确的是
| A.7.8 g Na2O2中含有的阴离子数目为0.2 NA |
| B.3.2 g O2和O3的混合气中含有的氧原子数目为0.2 NA |
| C.1 L 0.1 mol/L的 Al2(SO4)3溶液中,Al3+的数目为0.2 NA |
| D.过氧化氢分解制得标准状况下1.12 L O2,转移电子数目为 0.2 NA |