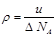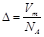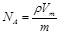设NA为阿伏加德罗常数,下列说法中正确的是
A.标准状况下,密度为d g/L的某气体纯净物一个分子的质量为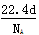 g g |
| B.常温常压下,17g甲基(—14CH3)所含的中子数为9NA |
| C.25℃时,1 L pH=13的NaOH溶液中含有NA个氢氧根离子 |
| D.4.6 g Na在空气中完全反应生成Na2O、Na2O2,转移0.2NA个电子 |
将Na2O2、HCl和Al2O3一起溶于一定量的水中,完全反应后,测得所得溶液中只含有Na+、AlO2-、Cl-(不考虑AlO2-的水解和H2O的电离),则Na2O2、HCl、Al2O3的物质的量之比不可能的是
| A.2;2;1 | B.3;3;1 | C.3;4;1 | D.4;6;1 |
下列表示物质的化学用语正确的是
A.NH4H的电子式: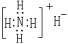 |
B.硝基苯的结构简式: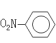 |
| C.葡萄糖的化学式:CH2O |
D.甲烷分子的比例模型: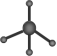 |
下列对应的表达方式错误的是
A.Cl-的结构示意图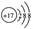 | B.2—甲基丁烷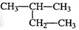 |
C.碳-12原子 C C | D.硫离子的核外电子排布式 1s22s22p63s23p4 |
有4.8g CuO、Fe2O3混合物跟足量CO充分反应后固体减少1.28g,反应后全部气体用0.6mol/L Ba(OH)2溶液100mL吸收。下列有关叙述中正确的是
| A.原混合物中CuO与Fe2O3物质的量的比为l:l |
| B.原混合物中CuO与Fe2O3的质量比为2:1 |
| C.吸收CO2后的溶液中一定有Ba(HCO3)2 |
| D.吸收CO2后的溶液中生成白色沉淀的质量为11.82 g |
FeS2在空气中充分燃烧的化学方程式为4FeS2 + 11O2 2Fe2O3 + 8SO2,若agFeS2在空气中充分燃烧,并转移N个电子,则阿伏加德罗常数(NA)可表示为
2Fe2O3 + 8SO2,若agFeS2在空气中充分燃烧,并转移N个电子,则阿伏加德罗常数(NA)可表示为
| A.120N/a | B.120a/11N | C.11a/120N | D.120N/11a |
镁铝碱式盐对工业污水中的铬有良好吸附性。取该碱式盐0.7525g,滴加1.0mol/L盐酸,当加盐酸21.25mL时开始产生CO2气体,加入盐酸至22.50mL时恰好反应完全,向该溶液中加入过量氢氧化钠溶液,过滤,沉淀物进行干燥后重0.4350g。则该碱式盐的化学式是
| A.Al2Mg6(OH)16CO3?4H2O | B.Al4Mg12(OH)34CO3?8H2O |
| C.Al2Mg4(OH)16CO3?4H2O | D.Al3Mg6(OH)34CO3?8H2O |
一种新的储氢方法,其原理是NaHCO3+ H2 HCOONa+ H2O。下列叙述正确的是
HCOONa+ H2O。下列叙述正确的是
| A.储氢、释氢的过程均无能量变化 |
| B.NaHCO3、HCOONa均含有离子键和共价键 |
| C.储氢过程中NaHCO3被氧化 |
| D.释氢过程中每消耗0.1molH2O放出2.24L的H2 |
有关物质结构的表述错误的是
| A.氯乙烯的结构简式:CH2="CHCl" |
B.氮分子的结构式: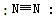 |
| C.氨分子的空间构型:三角锥形 |
| D.氯离子的最外层电子排布式:3s23p6 |