下列化学用语或模型表示正确的是
A.硝基苯的结构简式: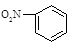 | B.CO2分子比例模型: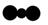 |
C.NH4Cl的电子式: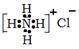 | D.NaCl的晶体模型: |
以下最接近阿伏加德罗常数的是
| A.2.0L 1.0mol·L—1 CH3COOH溶液中的H+离子数 |
| B.2.0L1.0 mol·L—1CH3COONa溶液中的CH3COO—离子数 |
| C.1.0L 1.0 mol·L—1NaHCO3溶液中的HCO3—离子数 |
| D.1.0L1.0 mol·L—1Na2CO3溶液中的 CO32—离子数 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
| A.25℃时,pH=1的1.0 LH2SO4溶液中含有的H+的数目为0.2NA |
| B.标准状况下,2.24 LCl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA |
| C.室温下,21.0 g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA |
| D.取0.5 L 0.2 mol·L-1mol氯化铁溶液 ,所得溶液含有0.1 NA个Fe3+ |
下列化学用语表示正确的是
A.CO2的比例模型: |
B.铝离子的结构示意图: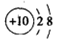 |
| C.次氯酸的结构式:H-Cl-O |
D.甲基的电子式: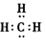 |
将35.8g Al、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生6.72L气体(标准状况)。另取等质量的该合金溶于过量的稀硝酸中,生成13.44L NO(标准状况),向反应后的溶液中加入足量的NaOH溶液,得到沉淀的质量为
| A.66.4 g | B.50.8 g | C.44.8g | D.39.2g |
在t ℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g·mL-1,质量分数为w,其中含有NH4+的物质的量是b mol,下列叙述正确的是( )
A.溶质的质量分数w=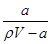 ×100% ×100% |
B.溶质的物质的量浓度c= mol·L-1 mol·L-1 |
C.溶液中c(OH-)=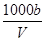 mol·L-1+c(H+) mol·L-1+c(H+) |
| D.向上述溶液中加入V mL水,所得溶液的质量分数大于0.5w |
下列关于物质的量、摩尔质量的叙述中正确的是( )
| A.0.012 kg12C中含有约6.02×1023个碳原子 |
| B.1 mol H2O中含有2 mol氢和1 mol氧 |
| C.氢氧化钠的摩尔质量是40 g |
| D.2 mol水的摩尔质量是1 mol水的摩尔质量的2倍 |
设NA为阿伏加德罗常数的值,下列叙述不正确的是( )
| A.常温下,4 g CH4含有NA个C—H共价键 |
| B.常温常压下,7.0 g乙烯与丙烯的混合物中含有氢原子的数目为NA |
| C.含有6.02×1023个中子的D2O的质量为2.0 g |
| D.1 mol Al3+完全水解生成Al(OH)3胶体粒子的数目为NA |
下列有关化学用语表示正确的是
| A.12753I和12953I2互为同位素 |
B.NH5的电子式为 |
C.氯原子的结构示意图: |
| D.中子数为146、质子数为92的铀(U)原子14692U |
下列说法正确的是
| A.0.5mol SO2和11.2LCO2所含的分子数目一定相等 |
| B.25℃和100℃时,水的pH相等 |
| C.中和等体积、等物质的量浓度的NaOH和氨水所消耗的n(H2SO4)相等 |
D.2SO2(g)+O2(g) 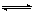 2SO3(g) 和4SO2(g)+2O2(g) 2SO3(g) 和4SO2(g)+2O2(g) 4SO3(g)的△H相等 4SO3(g)的△H相等 |