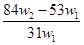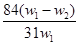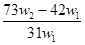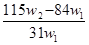设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.1 molCl2与足量Fe反应转移电子数一定为3NA |
| B.标准状况下,2.24 L NH3中含有共价键的数目为NA |
| C.1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3 NA |
| D.标况下,11.2 L SO3所含的分子数目为0.5NA |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.1 molCl2与足量Fe反应转移电子数一定为3NA |
| B.标准状况下,2.24 L NH3中含有共价键的数目为NA |
| C.1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3 NA |
| D.标准状况下,11.2 L SO3所含的分子数目为0.5NA |
等物质的量的N2、O2、CO2混合气体通过Na2O2后,体积变为原体积的8/9(同温同压),这时混合气体中N2、O2、CO2的物质的量之比为
| A.3:4:1 | B.3:3:2 | C.6:7:3 | D.6:9:0 |
过氧化钠与CO2作用,反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2↑。当0.2molNa2O2与足量CO2完全反应后,下表对生成物Na2CO3和O2的描述中正确的是
| | Na2CO3的质量 | 关于O2的描述 |
| A | 21.2g | O2的摩尔质量是36g·mol-1 |
| B | 21.6g | 生成标准状况下O2的体积为2.24L |
| C | 21.6g | O2的摩尔质量是34g·mol-1 |
| D | 22.4 g | 生成标准状况下O2的体积为2.24mL |
一定量CO2通入某浓度的NaOH溶液得溶液A,向A溶液中逐滴滴入稀盐酸,加入n(HCl)与生成n(CO2)的关系如图所示.下列有关叙述正确的是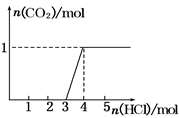
| A.通入的CO2气体为22.4 L |
| B.A溶液中n(NaOH)=2n(Na2CO3) |
| C.A溶液中既含Na2CO3,又含NaHCO3 |
| D.A溶液中一定只有Na2CO3 |
20g由两种金属粉末组成的混合物,与足量的盐酸充分反应后得到11.2L氢气(标准状况),这种金属混合物的组成可能是
| A.Mg和Al | B.Al和Fe |
| C.Fe和Zn | D.Zn和Cu |
Ⅰ、甲同学欲配制0.55 mo1·L—1 的NaOH溶液200mL(存在200mL容量瓶)。称量操作如下:
①先用托盘天平称量烧杯的质量。称量前先调节天平零点。用“↓”表示在天平右盘上放置砝码,用“↑”表示从天平右盘上取下砝码。取用砝码情况和游码读数如下:
| 砝码质量 | 50 | 20 | 20 | 10 | 5 |
| 取用砝码情况 | 先↓后↑ | ↓ | 先↓后↑ | ↓ | 先↓后↑ |
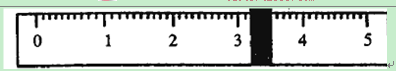
烧杯的质量为 g。
②称量烧杯和NaOH固体的质量。再在天平右盘上放置 g砝码,将游码的位置移到 g的位置,往烧杯中逐渐加入NaOH固体,直到天平达到平衡。
Ⅱ、乙同学欲用用18mol/L 浓硫酸配制100 ml 3.0mol/L 稀硫酸的实验步骤如下:
① 计算所用浓硫酸的体积 ② 量取一定体积的浓硫酸 ③ 溶解 ④ 转移
⑤洗涤 ⑥定容 ⑦摇匀
回答下列问题
(1)所需浓硫酸的体积是 ,量取浓硫酸所用的量筒的规格是 (请填编号)(从下列中选用 A.10ml B.25ml C.50ml D.100ml)
(2)定容时俯视溶液的凹液面对所配制的稀硫酸浓度有何影响
(用偏大、偏小、无影响填写)
用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.1molFeCl3与沸水反应生成胶体后,含有NA个Fe(OH)3胶粒 |
| B.标准状况下,1.12 L的HCHO所含的原子数是0.2NA |
| C.1 L0.5mol·L-1Na2CO3溶液中含有的CO32-数目为0.5NA |
| D.0.1 mol Na2O2作供氧剂时转移的电子数目是0.2 NA |
下列选项中所涉及到的两个量的一定相等的是
| A.11. 2LCl2与4.25gNH3所含有的原子数 |
| B.18.0g重水(D2O)与20gNe所含有的电子数 |
| C.标准状况下36gH2O与1.204×1024个O2分子所占的体积 |
| D.等物质的量的Al分别与足量的盐酸、NaOH溶液反应转移的电子数 |