设NA为阿伏伽德罗常数的值。下列叙述正确的是
| A.1mol甲醇中含有C—H键的数目为4NA |
| B.25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| C.标准状况下,2.24L己烷含有分子的数目为0.1NA |
| D.常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.4NA |
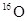 和
和 是氧元素的两种核素,
是氧元素的两种核素,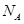 表示阿伏伽德罗常数,下列说法正确的是
表示阿伏伽德罗常数,下列说法正确的是
A.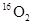 与 与 互为同分异构体 互为同分异构体 |
B.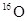 与 与 核外电子排布方式不同 核外电子排布方式不同 |
C.通过化学变化可以实现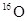 与 与 间的相互转化 间的相互转化 |
D.标准状况下,1.12L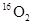 和1.12L 和1.12L 均含有0.1 均含有0.1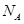 个氧原子 个氧原子 |
下列有关定量判断正确的是
| A.18gH218O分子中含有的10NA个质子 |
| B.将3mol NO2完全溶于水,生成NO气体,气体的物质的量变为2mol |
| C.将1.5molCO2气体通入到1L 1mol/L的NaOH溶液中,生成1mol碳酸钠 |
| D.2Cu2S+2H2SO4+5O2=4CuSO4+2H2O反应中,当1mol O2发生反应时,还原剂所失电子的物质的量 |
下列化学用语正确的是( )
| A.乙烯的比例模型: |
| B.HClO的结构式:HClO |
C.H2O2的电子式: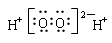 |
| D.乙醇的分子式:CH3CH2OH |
20℃时,饱和KCl溶液的密度为1.174 g·cm-3,物质的量浓度为4.0 mol·L-1,则下列说法中不正确的是
| A.20℃时,饱和KCl溶液与等质量的水混合后物质的量浓度大于2.0 mol·L-1 |
| B.20℃时,将29.8 gKCl溶于87.6 g水中可得饱和溶液 |
| C.20℃时,密度小于1.174 g·cm-3的KCl溶液是不饱和溶液 |
| D.将此溶液蒸发部分水,再恢复到20℃时,溶液中各离子的浓度不变 |
有一定体积CH4、C2H6、C3H8组成的混合气体,是同温同压下H2密度的15倍。则混合气体中CH4、C2H6、C3H8的体积比不可能是:
| A.2∶1∶2 | B.2∶3∶1 | C.1∶4∶1 | D.5∶3∶5 |
设NA为阿伏加德罗常数的值,下列有关叙述正确的是
| A.1 mol羟基所含的电子总数为10NA |
| B.标准状况下,1L正戊烷完全燃烧所生成的CO2分子数为5NA/22.4 |
| C.4.2g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
| D.1 mol碳正离子(CH3+)所含的电子总数为8NA |
某烷烃和烯烃的混合气体的密度是1.07 g·L-1(标准状况),该烷烃和烯烃的体积比是4∶1。这两种烃是
| A.CH4、C2H4 | B.C2H6、C2H4 | C.CH4、C4H8 | D.CH4、C3H6 |
乙烯的产量是衡量一个国家石油化工发展水平的重要标志。下列有关表述正确的是
A.乙烯的电子式是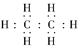 |
| B.乙烯的结构式为CH2CH2 |
C.乙烯中碳原子的结构示意图为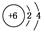 |
| D.5.6L乙烯中含有1mol C—H键 |
有五瓶溶液分别是:①10mL 0.60moL·L-1NaOH溶液 ②20mL 10.50moL·L-1H2SO4溶液 ③30mL0.40moL·L-1HCl溶液 ④40mL0.30moL·L-1CH3COOH溶液 ⑤50mL
0.20moL·L-1蔗糖水溶液。以上各瓶溶液所含离子、分子总数的大小顺序是
| A.⑤>④>③>②>① | B.②>①>③>④>⑤ |
| C.②>③>④>①>⑤ | D.①>②>③>④>⑤ |