题目内容
乙烯的产量是衡量一个国家石油化工发展水平的重要标志。下列有关表述正确的是
A.乙烯的电子式是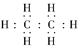 |
| B.乙烯的结构式为CH2CH2 |
C.乙烯中碳原子的结构示意图为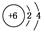 |
| D.5.6L乙烯中含有1mol C—H键 |
D
解析试题分析:一个乙烯分子应含有四个氢原子,碳碳之间是两对共用电子对,所以A错。结构式中碳氢键和碳碳双键必须画出来,所以B错。乙烯中的碳原子周围有8个电子而最外层应有6个电子C错。1mol乙烯含有4mol碳氢键,5.6L既是0.25mol恰好含有1mol 所以D正确。
考点:考查化学键及电子式,结构式,原子结构示意图的书写方法。

练习册系列答案
相关题目
NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A.7.8 gNa2S固体和7.8 gNa2O2固体中含有的阴离子数目均为0.1 NA |
| B.0.1mol·L-1的NaHSO4溶液中含有阳离子的物质的量为0.2mol |
| C.常温常压下,氧原子总数为0.2NA的SO2和O2的混合气体,其体积约为2.24 L |
| D.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA |
用NA表示阿伏加德罗常数,下列叙述正确的是
| A.标准状况下,22.40 L H2O含有的分子数为NA |
| B.常温常压下,1.06 gNa2CO3含有的Na+离子数为0.02NA |
| C.通常状况下,NA个CO2分子占有的体积为22.40L |
| D.物质的量浓度为0.50mol/L的MgCl2溶液中,含有C1-个数为NA |
下列所得溶液的物质的量浓度等于0.1 mol·L-1的是
| A.将0.1 mol氨气充分溶解在1 L水中 |
| B.将10g 1 mol·L-1的硫酸与90 g水混合 |
| C.将8g三氧化硫溶于水并配成1 L溶液 |
| D.将16g CuSO4·5H2O溶于水并配成1 L溶液 |
下列说法正确的是
| A.摩尔是物质量的单位 | B.标况下,1molNH3的质量才是17g |
| C.氦气的摩尔质量是4g/mol | D.1mol气体所占的体积约为22.4L |
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,5.6 L一氧化氮和5.6 L氧气混合后的分子总数为0.5NA |
| B.1 mol乙烷分子含有8NA个共价键 |
| C.58.5 g的氯化钠固体中含有NA个氯化钠分子 |
| D.在0.1 mol过氧化钠固体中,阴离子总数等于0.1 NA |
同温同压下,等质量的O2和O3相比较,下列结论正确的是( )
| A.它们的分子数目之比是 1∶1 | B.它们的氧原子数目之比为 2∶3 |
| C.它们的密度之比为 2∶3 | D.它们的体积之比是 1∶1 |
下列化学用语正确的是( )
| A.乙烯的比例模型: |
| B.HClO的结构式:HClO |
C.H2O2的电子式: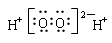 |
| D.乙醇的分子式:CH3CH2OH |